Термодинамическая концепция
Cтраница 1
Термодинамическая концепция запрещает такие динамические микромодели реальных объектов, которые нарушают основные аксиомы термодинамики. Следовательно, на классическую или квантовую механику накладываются определенные ограничения. Запрещаются, например, системы, не имеющие минимальной энергии или системы с такими дальнодействующими силами взаимодействия, для которых невыполнима аксиома аддитивности. [1]
Термодинамическая концепция, безусловно, правильно намечает основные черты явления. [2]
Основная термодинамическая концепция в процессах разделения состоит в представлении о переводе системы из начального состояния в заданное граничное состояние через последовательный непрерывный ряд равновесных состояний. [3]
Согласно термодинамической концепции все основные постулаты термодинамики, перечисленные в § 1, должны выполняться для любых макроскопических систем. Нарушение некоторых из этих постулатов, например закона возрастания энтропии, возможно лишь для весьма малых систем, содержащих небольшое число молекул, для которых лишь и возможны заметные относительные флуктуации. Следовательно, в любых макроскопических, адиабатически изолированных объектах энтропия может только возрастать или, достигнув максимального значения, оставаться неизменной. Иначе говоря, все макроскопические необратимые процессы протекают так, что с течением времени, отсчитываемом в одном и том же направлении, все макроскопические системы переходят от состояний менее равновесных к состояниям более равновесным. Противоположно направленные во времени макроскопические процессы исключаются термодинамической концепцией. [4]
В термодинамической концепции [42-44] закономерности ГПХ-процесса выводятся в условиях равновесности, делается попытка учесть конформационные изменения макромолекул при переходе из одной фазы в другую. [5]
Итак, термодинамическая концепция предполагает абсолютную справедливость принципа причинности и представления о необратимой направленности во времени любых макроскопических процессов. Сама эта концепция может быть представлена как вытекающая из постулата необратимой направленности времени, который можно рассматривать как дополнительную аксиому, уточняющую представление о времени, вытекающее из механики и других обратимых законов микродвижения. При таком подходе термодинамическая концепция эмоционально аргументируется нашими чувственно наглядными представлениями о необратимом течении времени. [6]
Поскольку приложимость термодинамических концепций к процессам развития подвергается сомнению ( Волькенштейн, 1975; 1981), заслуживают внимания другие подходы к обсуждаемой проблеме. Вир ( 1965) исходит из того, что противоречие между сохранением самотождественности и развитием связано не столько с организацией биосистем, сколько с нашей возможностью их познания. Для того чтобы противоречие снять, биосистему следует описывать с помощью двух модельных языков. В пределах языка № 1 биосистема замкнута и гомеостатична, в пределах языка № 2 она разомкнута и гомеоретична. Таким образом, язык № 2 способен обсуждать в терминах эквифинальности поведение замкнутого регуляторного контура, который сам по себе не является эквифинальным. [7]
Если исходить из термодинамической концепции, согласно которой второе начало не может быть нарушено для макроскопических процессов, то необратимая направленность макроскопических процессов и принцип причинности должны рассматриваться как ненарушимые в макромире. Лишь в микромире для элементарных процессов взаимодействия отдельных частиц эти представления могут оказаться бессодержательными, так как микроскопическая обратимость выступает в этой области как один из основных принципов, лежащих в основе законов микродвижения. [8]
Область применимости таких термодинамических концепций, как энтропия и свободная энергия, постепенно сужается и исчезает. [9]
Действуя в рамках довольно ограниченных термодинамических концепций того времени, он указал, что тепло не может выделяться в экспериментах по кручению, поскольку объем не меняется. [10]
Очевидно, принимая термодинамическую концепцию, надо отказаться от постановки вопроса об определении границ применимости классической термодинамики к макроскопическим системам. Ибо, согласно этой концепции, отступление от классической термодинамики возможно лишь в микроскопических масштабах, когда система содержит относительно небольшое число степеней свободы. [11]
 |
Значения поверхностного натяжения и термодинамической работы адгезии различных материалов. [12] |
В последние годы получила наибольшее распространение термодинамическая концепция, в рамках которой основная роль отводится соотношению поверхностных энергий адгезива и субстрата. [13]
Гиббс исследует вопрос о соотношении между механическими и термодинамическими концепциями и разрабатывает общий, мощный метод, позволяющий, по меньшей мере принципиально, исследовать все важнейшие задачи данного цикла. [14]
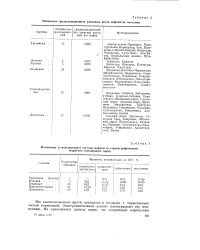 |
Изменение средневзвешенных удельных весов нефтей по системам. [15] |
Страницы: 1 2 3