Диаграмма - система
Cтраница 1
Диаграмма системы характеризуется двумя полями первичных выделений: поле твердых растворов сульфидов свинца и олова и поле твердых растворов хлористых солей. Поле твердых растворов сульфидов занимает большую часть концентрационного квадрата. Все изотермы, пересекающие стабильную диагональ РЬСЬ - SnS, распадаются на две ветви. Образование устойчивой пары солей РЬСЬ и SnS из SnClz и PbS сопровождается выделением 4 8 ккал тепла. [1]
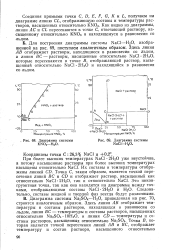 |
Диаграмма системы NaCl - Н2О. [2] |
Диаграмма системы Na2SQ4 - H2O, приведенная на рис. 70, строится аналогичным образом. [3]
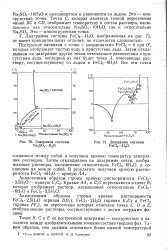 |
Диаграмма системы Na2SO4 - Н2О.| Диаграмма системы. РеС13 - Н20. [4] |
Диаграмма системы РеС13 - Н2О, изображенная на рис. 71, не имеет принципиальных отличий, но отличается сложностью. [5]
Диаграмма системы гликоль додеканол 1-нитроэтан, для которой характерно образование при определенных температурах множества гомогенных и гетерогенных областей. [6]
Диаграмма системы СаО - НЮ2 сходна с диаграммой СаО - ZrO2; в ней образуются стабильные твердые растворы с кубической решеткой. [7]
Диаграмма системы гликоль додеканол 1-нитроэтан, для которой характерно образование при определенных температурах множества гомогенных и гетерогенных областей. [8]
Диаграмма системы, в которой при данной температуре существует одна двойная безводная соль, образованная из двух безводных солей, отличается от диаграммы простейшего типа ( рис. 114, стр. [9]
Диаграммы систем, состоящих из двух компонентов и образующих между собой одно или несколько химических соединений, построены по тому же самому правилу, что и диаграммы систем, не образующих между собой химических соединений, но они обладают некоторыми особенностями построения. Представленная в общем виде система состоит из двух компонентов А и В. Она имеет две эвтектические точки О и Ot и один максимум АВ. Максимум показывает, что компоненты А и В образуют химическое соединение. Первая эвтектическая точка О соответствует эвтектике веществ А и АВ, вторая точка Ох соответствует эвтектике веществ А В и В. [10]
Диаграмма системы SiO2 - A12O3 впервые была опубликована Шепердом, Ранкиным и Райтсм в 1909 г. Затем в 1924 г. она была исправлена Боуэном и Грейгом. В последнем варианте диаграмма и до настоящего времени помещается в специальной и технической литературе. [11]
Диаграмма системы СаО - SiO2 в целом представляет собой как бы комбинацию, составленную из диаграмм перечисленных систем. [12]
 |
Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся инконгруэнтно. [13] |
Диаграмма системы с химическим соединением, плавящимся инконгруэнтно ( рис. 16), характеризуется одной двойной эвтектикой Е между компонентами А и АтВп и наличием слабо выраженного перегиба и на кривой ликвидуса. [14]
 |
Кривые зависимости между свободной энергией и температурой. а - Энантиотропная система. б - монотропная система. [15] |
Страницы: 1 2 3 4