Тетраэдрическая координация
Cтраница 1
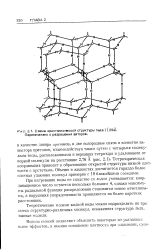 |
Схемы кристаллической структуры льда.. Перепечатано с разрешения авторов. [1] |
Тетраэдрическая координация приводит к образованию открытой структуры низкой плотности с пустотами. Обычно в жидкостях достигается гораздо более плотная упаковка молекул примерно с 10 ближайшими соседями. [2]
Тетраэдрическая координация в соединениях кадмия встречается очень редко. [3]
Тетраэдрическая координация встречается, в общем, довольно редко. Она найдена в некоторых соединениях Си с полидентатнымн органическими лигандами и в четком виде - в галогенидах ( хлоридах и бромидах) меди с крупными катионами. Некопланарное расположение связей в некоторых внутрикомплекеных соединениях вызывается, возможно, требованиями, налагаемыми на валентные углы и длины связей в металлоциклах. Однако в другом соединении Си с полидентатными лигандами - комплексе меди с имида-золом Cu ( C3H3N2) 2 ( 129 ] - лишь половина молекул имеет ис-каженно-тетраэдрическую координацию; в другой половине молекул координация Си плоскостная. [4]
Тетраэдрическая координация превалирует в комплексах с одной тг-органической системой, особенно в смешанных карбонильных тг-органических комплексах. [5]
Тетраэдрическая координация имеется у многочисленных структур, причем различные структурные типы отличаются друг от друга лишь способом сочленения тетраэдров в кристаллическом пространстве. Если у SnCl2 и BeF2 трехмерное ( каркасное) соединение тетраэдров, то у SiS2 и ВеС12 тетраэдры соединены в бесконечные ( параллельно расположенные) цепи. Поэтому в табл. 49 систематизированы представители кристаллов состава АВ2 с координационными полиэдрами в виде тетраэдров. [6]
Тетраэдрическая координация характерна и для гидратированных солей аналогичного состава: молекулы воды не входят во внутреннюю сферу молибдена и вольфрама. В частности, в Na2Mo04 - 2H20 [85] они связывают тетраэдры [ Мо04Р - в гофрированные слои, между которыми располагаются ионы натрия. [7]
Тетраэдрическая координация характерна и для большинства двойных молибдатов и вольфраматов трех - и одновалентных металлов. [8]
Тетраэдрическая координация в метаборатах не ограничивается только модификациями, существующими при высоких давлениях. [9]
Тетраэдрическая координация Cd была недавно найдено и в Qui2 - [ СиСЦ ] [527], где Qui - хянолшшй. [10]
Тетраэдрическая координация As несколько искажена: углы С-As - С 104 ( 1) уменьшены, а углы Fe-As - С 114 ( 1) увеличены в сравнении с идеальным, что вообще характерно для комплексов арсинов, а также аминов, фос-финов и стибинов. [11]
Тетраэдрическая координация кобальта, найденная в структурах Na2 [ Co ( NCS) 4 ] - 8H2O, K2 [ Co ( NCS) 4 ] ЗН2О [61, 75], [ HgTu4 ] [ Co ( NCS) 4 ], Hg ( SCN) 4Co, Hg ( SeCN) 4Co, находится в согласии с представлением о стереохимическом сходстве тио - и селеноцианатных соединений с хлоридами и бромидами. Лишь в Hg2 ( SCN) 6Co С6Н6 атом кобальта координирует не четыре, а шесть роданогрупп. [12]
Тетраэдрическая координация Asv атомами кислорода уже найдена в арсиновых кислотах R-AsO ( OH) 2 [ И ] и в диметил-арсиновой кислоте ( CH3) 2AsO ( OH) [ 12J, молекулы которой с помощью водородных связей образуют в кристаллах димеры, подобные димерам карбоновых кислот. [13]
Тетраэдрическая координация Hg ( II) атомов галогена реализуется лишь в одном из днгалогенидов ( в красной модификации HgI2), но она характерна для таких комплексных галоге-нидов, как Ag2HgI4 л Cu2HgI4 ( разд. Отме-тим большое различие в длинах связей hg - C1 при образовании двух коллпнеарных связей ( 2 3 А) и значением 2 5 А для тет-раэдрически направленных связей. [14]
Тетраэдрическую координацию никель имеет, по-видимому, и в некоторых других классах внутрикомплексных соединений. Во многих других внутри-комплексных соединениях никеля с узлами № О4 осуществляется октаэдрическая координация. [15]
Страницы: 1 2 3 4