Сильная координация
Cтраница 1
Сильная координация между простыми эфирами и соединениями Гриньяра говорит о том, что последние обладают свойствами кислот Льюиса. [1]
В случае сильной координации в XXXVII ( например, в неполярных растворителях или в присутствии лития) вращение вокруг связи между углеродами 2 и 3 на конце цепи невозможно, что и приводит к цис - l 4-полимеризации. В слабо координированном комплексе, который допускает вращение вокруг связи, идет транс-и г ис-1 4-полимеризация. [2]
Исключение, проявляющееся во втором примере, связано с сильной координацией лития и большей основностью атома азота N ( i в неполярном растворителе, что приводит к дополнительной активации положения 2 к нуклеофильной атаке и, вероятно, обеспечивает возможность реали-внутримолекулярного процесса. В присутствии кислот образуется смесь возможных метоксипроизводных приблизительно в равных количествах. [3]
Вторая группа должна быть протоне донором, т.е. иметь подвижный протон, после удаления которого возникающий анион способен вступать в сильную координацию с ионом металла. [4]
 |
ИК-спектры кислых ЭДТА-тов La различного гидратного состава. [5] |
При дегидратации HLaA - 7H2O до HLaA - H2O полоса vco сдвигается до 1670 см-1, что связано с усилением координации карбоксильной группы. Полная дегидратация приводит к еще более сильной координации. Связь протона в СООН-группе становится ионной, он теряет свое постоянное место на одном из атомов кислорода ЭДТК, и полосы vco не проявляются. [6]
Гидрирование протекает медленно, однако образование алканов или циклоалканов не отмечено. То, что реакция останавливается на стадии алкеновых соединений, указывает на сильную координацию ал-ленов. Вместе с тем известно, что алленовые соединения легко реагируют с гндридными комплексами. [7]
Различие заключается в том, что в случае реакции SN2 входящая и уходящая группы так сильно координированы с атомом углерода, что уходящая группа не может заместиться другим нуклеофи-лом, прежде чем произойдет превращение в продукты реакции. Таким образом не может образоваться симметрично построенная частица, и наблюдается обращение. Столь сильная координация означает также, что центральный атом углерода не приобретает заметного положительного заряда. В случае сольва-тированного иона карбония время жизни промежуточной частицы достаточно велико для того, чтобы другая молекула растворителя успела заменить уходящую группу. Координация в этом случае достаточно слаба, так что есть основания считать, что атом углерода несет полный положительный заряд. [8]
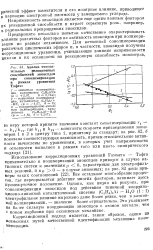 |
Анализ относительных реакционных способностей эпоксидов при сополимеризации в рамках уравнения Тафта. [9] |
Все остальное многообразие процессов, где перекрывается действие многих факторов, занимает здесь промежуточное положение. Однако, как видно из рисунка, при сополимеризации эпоксидов под действием типичной координа - Ционно-аииопной каталитической системы ( С2Н3) оА1 - Н20 ( 1: 1) электрофильное влияние выражено даже более резко, чем в катион - Ной полимеризации, - значение более отрицательно. Это указывает На более сильную координацию эпоксидов с атомом металла, чем с ионом карбония при оксониевом механизме. [10]
В ионной полимеризации с участием свободных растущих частиц факторы, определяющие стереохимию процесса, аналогичны тем, которые наблюдаются в радикальной полимеризации. Синдиотактическая конфигурация становится предпочтительной при понижении температуры реакции. Если же между инициатором, концом растущей полимерной цепи и мономером имеет место сильная координация, то положение в корне меняется. [11]
Многие результаты теоретических и экспериментальных работ по гидратации ионов ( некоторые из этих работ приведены в табл. 2 и 3) можно интерпретировать на основе современных представлений о структурных и динамических свойствах воды. Особый интерес представляет способность некоторых ионов разрушать структуру воды, образовывая с ней комплексы, включаться в существующую структуру воды, увеличивать или уменьшать степень упорядочения растворителя на значительном расстоянии. Ионы классифицируются как структуроразрушители и структурообразователи в зависимости от того, разрушают ли они структуру воды с образованием менее специфической структуры со слабой координацией молекул, стабилизируют существующую структуру или же приводят к новой гидратной структуре с сильной координацией. Однако такое разделение не всегда оправдывается в различных измерениях. В настоящее время почти нет сомнений в том, что в растворе могут существовать гидратиро-ванные группы со специфической локальной координацией ионов и молекул воды. Некоторые ионы могут разрушать структуру воды путем комбинации кулоновсксто взаимодействия, поляризационных и стерических факторов. Так, имеются свидетельства того ( табл. 3), что ионы с сильными полями образуют гидратные комплексы с ближним порядком, аналогичным порядку в соответствующих кристаллогидратах, но с различной степенью ковалентного связывания иона металла с кислородом воды. Сильные поля таких ионов могут вызывать упорядочение растворителя за первым гидратным слоем. Имеются также данные, указывающие на то, что при низких концентрациях и температурах водоподобные области могут сосуществовать с гидратиро-ванными ионами. Очевидно также, что в некоторых случаях ( табл. 3) ионы могут включаться ( путем внедрения или замещения) в существующую структуру воды и при этом не разрушать ее. [12]
Энтропии активации для гидролиза эфиров всегда отрицательны и их значения колеблются от - 20 до - 30 ккал. Полностью удовлетворительного количественного объяснения столь низким значениям энтропии не существует, однако несомненно, что важным эффектом является частичное связывание молекул воды в переходном состоянии, что вызывается высоким диполярным характером активированного комплекса. Изменения энтропии в процессе ( 1), вероятно, очень малы, но AS2 должно принимать сильно отрицательные значения, вызванные распределением зарядов в переходном состоянии. Следствием этого распределения является сильная координация с молекулами воды. [13]
Близкая картина наблюдается для wc-p - хлорвинилмеркурхло-рида. Мы уже отмечали, что для транс-производного обнаружено межмолекулярное взаимодействие р - атома хлора с атомом ртути, подтвержденное рентгеноструктурным исследованием. Поэтому естественно сравнивать расстояния между валентно несвязанными атомами для цис - и транс-соединений. Кратчайшее межмолекулярное расстояние С1 - - Hg в транс-хлориде, соответствующее наиболее сильной координации, равно 3 40 А. [14]
Как при сохранении, так и при нарушении копланарности металлоорганической группировки с ароматическим кольцом экранирование фтора возрастает в результате координации. Это обусловлено большей чувствительностью химического сдвига фтора к увеличению электронной плотности на сопряженном с кольцом заместителе в тг-положении, чем к ее эквивалентному уменьшению на заместителе в - положении. Необходимо отметить, что рост ХСЗ металлоорганических группировок при переходе от фторфенолятов к бромзамещенным аналогам можно было бы, по крайней мере в принципе, объяснить увеличением электроноакцептор-ной способности феноксильной группы при введении атомов брома. Сравнение относительного роста ХСЗ для группировок ( C6H6) 3SnO - и C6H5HgO - при переходе от 2-фторфенолятов к 2 6-дибромзамещенным показывает, что в последнем случае имеет место более сильная координация металлоорганической группировки с атомом галогена. Аналогичное рассуждение приводит к выводу, что образование внутримолекулярной водородной связи с атомом брома сопровождается меньшим переносом электронной плотности, чем в случае координации ртутноорганической группировки с атомом галогена. [15]
Страницы: 1 2