Октаэдрическая координация - металл
Cтраница 1
Октаэдрическая координация металла в димерном ацетилаце-тонате Со [ ОС ( СНз) СНС ( СН3) О ] 2 - Н2О 2 вполне естественна. Однако здесь имеется одна особенность. Причина такого различия не ясна. [1]
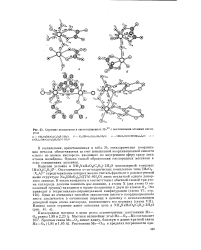 |
Строение комплексов в оксосоединениях Movl с мостиковыми атомами кислорода. [2] |
В соединениях, представленных в табл. 34, октаэдрическая координация металла обеспечивается за счет повышенной координационной емкости одного из атомов кислорода, входящего во внутреннюю сферу сразу двух атомов молибдена. Однако способ образования кислородных мостиков в этих соединениях различен. [3]
Другие комплексы, входящие в эту группу, также имеют октаэдрическую координацию металла, но содержат различные лиганды по оси октаэдра. В качестве модельных для нитрозилметаллопротеинов исследованы структуры Fe ( NO, 1 - MeIm) TPhP и Mn ( NO, 4 - MePy) TPhP [144], Эти соединения кристаллизуются в одной и той же пространственной группе. Атомы металлов имеют искаженную октаэдрическую координацию. Длины связи М - Nb с лигандами по оси октаэдра различны. Связь Fe-N с группой NO имеет длину 1.743 А, Мп-N 1.644 А. [4]
Здесь будет рассмотрено только АП лигандов в этих ХС с октаэдрической координацией металла. [5]
Молекулы обоих соединений являются биядерными комплексами с одиночными линейными кислородными мостиками и октаэдрической координацией металла. [6]
В 24 - х структурах выявлены одноядерные октаэдрические комплексы, в двух - двуядерные с октаэдрической координацией металла и только в одном - Co ( NO2) Cl - димерные комплексы с тетраэдрическим окружением атомов кобальта двумя группами NO и двумя мостиковыми атомами хлора. [7]
Комплекс [ МоОХ6 ] 2 может служить моделью электронной системы для всех других монооксогалогенидов молибдена ( с октаэдрической координацией металла) как островного, так и неостровного типа. Очевидно, что эффект трансвлияния кратной связи может проявляться независимо от того, являются ли лиганды ацидными или нейтральными донорными, концевыми или мостиковыми. [8]
Склонность атомов галогена к роли мостиков, связывающих атомы металла, могла бы привести к полимеризации молекул и осуществлению октаэдрической координации металла и в таких высокоспиновых соединениях, как Co ( DenMe) Cl2, Co ( Et4Dien) Cl2, Ca ( Paphy) Cl2, где DenMe ( CH3) N [ CH2CH2N - ( СНзЫа, Et4Dien HN [ CH2CH2N ( C2H5) 2 ] 2 Paphy С НюЫ4 Однако этого не происходит. [9]
В высокоспиновых соединениях Реш, так же как и в соединениях его электронного аналога Мп11 ( имеющих конфигурацию несвязывающих электронов d5), наиболее распространенной считается октаэдрическая координация металла. Значительно интереснее то, что в остальных шести внутрикомплексных соединениях координационное число железа оказалось равным пяти или семи. Тетрагонально-пирамидальная координация найдена в четырех соединениях, пентагонально-бипирамидальная - в двух. [10]
Представляется весьма важным исследовать кристаллическую структуру этого соединения и выяснить, каково расстояние Мо-Мо в комплексе и наблюдается ли в нем перегиб по линии О... Результаты этого исследования позволят выяснить, насколько общим является различие в способе обменного взаимодействия атомов металлов в сульфо - и оксокомплексах Mov при октаэдрической координации металла. [11]
Уменьшение радиусов от La до Lu проявляется также в том, что металлы из разных частей группы лантаноидов могут иметь разные координационные числа и разные кристаллические структуры. Например, атомы лантаноидов в трихлоридах La-Gd имеют координационное число 9, в то время как хлориды Tb-Lu обладают структурой типа А1С1з с октаэдрической координацией металла. Аналогичные различия наблюдаются для координационных чисел ионов в растворах. [12]
Подобно MoF5, NbF5, TaF5 и WOF4, пентафторид рутения построен из тетрамерных кольцевых молекул: четыре октаэдра RuF6 связаны друг с другом мостиковыми атомами фтора и образуют восьмичленный цикл, в котором чередуются атомы рутения и фтора. Атомы рутения двух сортов. При одинаковой октаэдрической координации металла ( два мостиковых атома фтора в ыс-положении и четыре концевых атома фтора) атомы Ru ( D и Ru ( 2) отличаются длинами связей Ru-РКОНц. [13]
На рис. 176 дало схематическое изображение тетрадентатного лиганда QAS и приведены основные расстояния и валентные углы. Заметно искажены и углы при Костиковых атомах углерода фенильных колец, соединяющих атомы As. Благодаря этим искажениям углов в лиганде становится возможной октаэдрическая координация металла. [14]
Химические свойства Mo W очень сходны, но значительно отличаются от свойств Сг; для них важны состояние окисления IV, V и VI, в то время как состояние окисления II практически неизвестно. Для обоих элементов характерно большое разнообразие геометрических конфигураций комплексов, причем имеется много примеров комплексов с координационными числами больше шести; например, [ Mo ( CN) 8 ] 4 -, [ Mo ( CN) 8 ] 3 - ( искаженный треугольный додекаэдр); полимерные окислы, сульфиды. Дискретный [ МоС4 ] 2 - существует в сильнощелочных растворах, а при подиис-лении образуются разнообразные изополимолибдаты или изополи-вольфраматы. Для этих соединений характерны октаэдрическая координация металла с атомами кислорода и различные типы общих углов или ребер. Относительно редки комплексы в состоянии окисления III, а для Мо и W в состояниях окисления IV, V и VI известны главным образом анионные комплексы. [15]
Страницы: 1