Диаграмма - состояние - однокомпонентная система
Cтраница 2
Представьте себе, что Вы знаете правило фаз Гиббса, изучили диаграммы состояния однокомпонентных систем, но не знакомы с диаграммами состояния двухкомпонентных систем. [16]
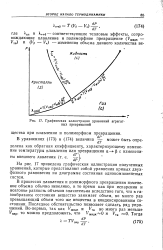 |
Графическая иллюстрация уравнений агрегатных превращений. [17] |
На рис. 17 приведена графическая иллюстрация полученных уравнений, которые представляют собой уравнения кривых двухфазного равновесия на диаграмме состояния однокомпонентных систем. [18]
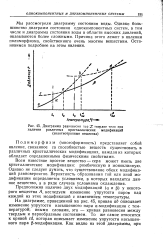 |
Диаграмма равновесия пар твердое тело при. [19] |
Однако большинство диаграмм состояния однокомпонентных систем, в том числе и диаграмма состояния воды в области высоких давлений, оказываются более сложными. Причина этого лежит в явлении полиморфизма, свойственного очень многим веществам. [20]
На рис. 44 а показана диаграмма состояния однокомпонентной системы. [21]
На рис. 16 - 1 показана диаграмма состояния воды. На рис. 16 - 2 показана диаграмма состояния однокомпонентной системы. [22]
Но при этом второй параметр - давление - должен изменяться не произвольно, а в определенной зависимости от температуры. Как мы уже видели во фрагменте 6 - 4, эта зависимость для различных комбинаций фаз ( различного фазового состава системы) выражается соответствующими кривыми на диаграммах состояний однокомпонентных систем. [23]
Критическим называется такое состояние, при котором жидкая фаза и ее насыщенный пар в состоянии равновесия имеют одинаковые физические свойства и отсутствует мениск на границе жидкость - пар. В критическом состоянии становятся равными плотности, а также удельные объемы жидкости и ее насыщенного пара. Теплота испарения в критическом состоянии равна нулю. На диаграммах состояния однокомпонентных систем ( рис. III.44) критическое состояние описывается так называемой критической точкой координаты которой представляют собой важные константы вещества, называются критическими параметрами и зависят от природы вещества. [24]
Критическим называется такое состояние, при котором жидкая фаза и ее насыщенный пар в состоянии равновесия имеют одинаковые физические свойства и отсутствует мениск на границе жидкость - пар. В критическом состоянии становятся равными плотности, а также удельные объемы жидкости и ее насыщенного пара. Теплота испарения в критическом состоянии равна нулю. На диаграммах состояния однокомпонентных систем ( рис. II 1.44) критическое состояние описывается так называемой критической точкой, координаты которой представляют собой важные константы вещества, называются критическими параметрами и зависят от природы вещества. [25]
С, соответствующие местам пересечения двух линий фазовых равновесий и лежащие поэтому на границе сразу трех гомогенных областей, называются тройными точками. Например, в точке О возможно сосуществование жидкой воды, пара и льда I. Координаты этой точки указаны на графике. Из рис. 6.2 видно, что на диаграмме состояний однокомпонентной системы нет областей ( точек), в которых число сосуществующих фаз может быть равно четырем или более. [26]
Страницы: 1 2