Коррозия - цинковый электрод
Cтраница 1
Коррозия цинкового электрода заключается во взаимодействии цинка с хлористым аммонием, примесями солей некоторых тяжелых металлов, водой или кислородом, растворенным в воде. Все перечисленные вещества входят в состав солевого электролита. [1]
Саморазряд элементов Лекланше связан главным образом о коррозией цинкового электрода. На этот процесс сильное влияние еказывают примеси, содержащиеся в цинке и электролите. [2]
При работе электрохимической системы с отбором тока столь отрицательное значение потенциала на цинковом электроде не достигается ( см. рис. VII-24), поэтому коррозии цинкового электрода за счет выделения водорода не происходит. [3]
В кислой зоне при тех же условиях работы электрохимической системы значения этого потенциала положи-тельнее - 1 В ( по НКЭ), что делает возможной коррозию цинкового электрода за счет выделения водорода. Коррозия цинка возможна даже несмотря на увеличение перенапряжения водорода при работе системы под током. [4]
Саморазряд марганцево-цинковых элементов с солевым электролитом достигает 30 % в год. Одной из причин саморазряда является коррозия цинкового электрода. [5]
Введением окиси цинка в раствор коррозия цинкового электрода сводится к минимуму. Для снижения скорости коррозии цинка отрицательного электрода элемента в некоторые электролиты дополнительно вводят двухромовокислый калий. [6]
Введением окиси цинка в раствор коррозия цинкового электрода ртутно-цинкового элемента сводится к минимуму. [7]
Амальгамация замедляет саморастворение цинка. Даже незначительное содержание ртути ( менее 1 %) снижает скорость коррозии цинкового электрода серебряно-цинкового аккумулятора в несколько раз. [8]
Можно считать, что в устройствах, где не предъявляется ] особых требований к стабильности напряжения и размерам. Оба этих вида батарей обладают хорошей сохраняемостью, их конструкция обеспечивает удаление газообразных про - j дуктов саморазряда, а коррозия цинкового электрода сни - жена. [9]
Сохранность ртутно-цинковых элементов достаточно высокая. Для большинства типов элементов гарантируется сохранность в течение 18 месяцев. При высоких температурах элементы могут быстро выходить из строя из-за коррозии цинкового электрода, приводящей к нарушению изоляции электродов. [10]
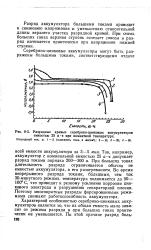 |
Разрядные кривые серебряно-цинковых аккумуляторов емкостью 25 а ч при комнатной температуре. [11] |
Так, например, аккумулятор с номинальной емкостью 25 а ч допускает разряд токами порядка 200 - 300 а. При больших токах длительность разряда ограничивается обычно не емкостью аккумулятора, а его разогреванием. Во время непрерывного разряда токами, большими, чем ток 30-минутного режима, температура поднимается до 90 - 100 С, что приводит к резкому усилению коррозии цинкового электрода и разрушению сепараторной пленки. Поэтому многократные разряды форсированными режимами снижают работоспособность аккумулятора. [12]
Суммарная элементная реакция без участия электролита позволяет свести его количество к минимуму, ограниченному пористостью электродов и габаритами сепараторов. В промышленных образцах элементов вводится около 1 0 мл электролита на 1 а ч номинальной емкости. В качестве электролита используется 35 - 40 % - ный раствор КОН, содержащий приблизительно 5 % растворенной окиси цинка. Использование цинкатного раствора, а не чистой щелочи уменьшает коррозию цинкового электрода и, кроме того, стабилизирует при разряде его потенциал. Таким электролитом пропитывают гигроскопичный материал, проложенный между электродами. Между адсорбирующей прокладкой и положительным электродом в ОР-элементах с жидким электролитом иногда помещают ионопроницаемый барьер типа пергамента, препятствующий попаданию частиц окиси ртути к аноду. [13]
На каждый ампер-час номинальной емкости элемента берется примерно 10 мл такого электролита. С медноокисным электродом на силикатном связующем такая примесь переходит в электролит, выщелачиваясь из положительной активной массы. При необходимости эксплуатации элементов в диапазоне температур - 30ч - 40 С их заливают 7 - 8 н раствором едкого кали, имеющим более низкую температуру замерзания, чем раствор едкого натрия. Расход раствора едкого кали на каждый ампер-час номинальной емкости может достигать 7 - 8 мл. В таком электролите при температурах выше 0 С отмечается, однако, несколько большая коррозия цинкового электрода. Заливка элемента электролитом производится на месте эксплуатации. Поверхность электролита экранируется тонким слоем минерального неомыляемого масла, что устраняет карбонизацию щелочного раствора, его испарение и ползучесть щелочи. [14]
Страницы: 1