Катодная коррозия
Cтраница 2
Большому содержанию в рециркуляционной воде растворенных твердых веществ соответствуют высокие электропроводность и коррозионные токи. В этом случае в коррозионном процессе могут принимать участие катодные участки, расположенные на значительном расстоянии от любой анодной точки, что приведет к расширению сферы катодной коррозии. [16]
Некоторые зарубежные исследователи ( Горман, Хорнунг) полагают, что катодная коррозия свинцовой оболочки кабелей происходит вследствие образования в зоне катода щелочной среды. Однако эта точка зрения неправильна, так как в щелочной среде, при соответствующей величине защитного потенциала ( - 0 42 в), и без перемешивания достигается высокий защитный эффект. В случае же катодной коррозии ободочка кабелей выходит из сцроя че рев 2 - 3 месяца и даж меньше. [17]
Минимальный защитный потенциал обеспечивает защиту металла от электрохимической коррозии. Потенциал не менее этого значения должен поддерживаться в конце защищаемого участка. Превышение максимального ( по абсолютному значению) защитного потенциала может привести к катодной коррозии оболочек кабеля и вызвать - коррозионное разрушение соседних подземных сооружений. [18]
Наибольшее влияние на потенциал других трубопроводов и кабелей обычно оказывают воронки напряжения над анодными заземлителями в системах катодной защиты, в которых имеется высокая плотность защитного тока и большой градиент потенциалов в грунте. Поскольку при этом происходит смещение потенциалов только в отрицательную сторону, опасности анодной коррозии не возникает. Однако в коррозионных системах группы II ( см. раздел 2.4), например для алюминия и свинца в грунте, все же может произойти катодная коррозия. [19]
Специальные городские комитеты, занимающиеся контролированием электролиза, имеют целью снижение коррозии от блуждающих токов. Большая величина тока, переходящего из железнодорожных систем в кабельные оболочки, может вызвать оседание щелочей на оболочке кабеля, например гидроокиси натрия, которые при определенных условиях могут вызвать катодную коррозию свинца. Когда дренажные токи слишком велики, свинцовые оболочки поляризуются до появления высокого отрицательного потенциала. [20]
После этого коррозия захватывает как щель, так и свободную поверхность титана и становится общей. Этот вид коррозии титана на поверхности, находящейся вне щели, вызываемый протеканием катодного тока, назван авторами [98] не вполне удачно катодной коррозией. IV, объясняется проявлением в этом случае отрицательного защитного эффекта. [21]
Наиболее ярко выражено явление перезащиты для таких металлов, как свинец и алюминий. Окислы этих металлов оказываются хорошо растворимы и в кислотах, и в щелочах. Окислы алюминия легко растворяются в щелочи с образованием алюминатов. Зависимость скорости растворения алюминия от плотности тока и потенциала приведена в табл. 45, а в табл. 46 и 47 сведены данные по катодной коррозии свинца в растворах хлористого калия ( различной концентрации) и в 0 1 н растворе NaOH. В последней таблице показано снижение скорости коррозии и последующее ее возрастание при высоких отрицательных потенциалах. [22]
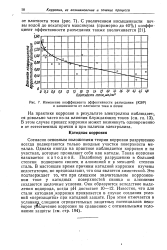 |
Изменение коэффициента эффективности разъедания ( КЭР и зависимости от плотности тока в почве. [23] |
Согласно основным положениям теории коррозии разрушению всегда подвергаются только анодные участки поверхности металла. Однако иногда на практике наблюдается коррозия и на участках, которые проявляют себя как катоды. Такая коррозия называется катодной. Подобному разрушению в большей степени подвержен свинец и алюминий и в меньшей степени сталь. В настоящее время причины катодной коррозии изучены недостаточно, но предполагают, что она является химической. Это подтверждает то, что при слишком значительном коррозионном токе у катодных поверхностей свинца и алюминия создаются щелочные условия. Известно, что для стали катодная t коррозия проявляется в случае создания условий пгрезащиты при катодной защите. При этом отмечается в условиях слишком отрицательных защитных потенциалов некоторое увеличение коррозии по сравнению с оптимальными условиями защиты ( см. стр. [24]
Утверждают иногда, что если металл является катодом по отношению к его окружению, то не произойдет никакого вреда. Это не совсем правильно, хотя катодное повреждение обычно меньше, чем анодное, и для железа, по крайней мере, его можно было бы и не принимать в расчет. В практике системы защиты, основанные на сохранении железных труб в катодном состоянии, имели, как уже было указано, успех в некоторых местностях. Тем не менее там, где вода имеет сравнительно много солей, образование гидроокиси натрия на железном катоде, уложенном в цемент или бетон, может размягчить цемент, а на свинцовом катоде щелочь может действовать на самый катод благодаря амфотерному характеру окислов свинца. Это случается главным образом там, где применяют соль, например, для оттаивания замерзших железнодорожных стрелок. В одном случае было замечено, что соль капала из тележки мороженщика. Гидроокись натрия, образовавшаяся на катодных местах, действует на свинец, давая натриевый плюмбит. Последний в результате гидролиза дает красный осадок, состоящий из микроскопических тетрагональных кристаллов моноокиси свинца, совершенно не похожий на коричневую перекись, образующуюся иногда на анодных участках. Травленая поверхность вследствие катодной коррозии имеет темный цвет, в противоположность блестящему виду анодно корродировавшего свинца. [25]
Страницы: 1 2