Атака - хлорид-ион
Cтраница 1
Атака хлорид-иона на другой концевой атом углерода приводит к конечному продукту. [1]
В случае несимметричного иона цикл раскрывался бы в соответствии с электронным фактором, т.е. при атаке хлорид-иона по более положительно заряженному атому С2, с образованием 1-иод - 2-метил - 2-хлорпропана - как и в реакции с участием открытого карбкатиона. [2]
В отсутствие растворителя образуется 2-хлороктан с 78 % - м обращением конфигурации, что определенно указывает на замещение хлорсульфитной группы в результате атаки хлорид-ионов с тыла. При термическом разложении 2-октилхлорсульфита в диоксане наблюдается сохранение конфигурации на 84 %, но этот результат следует рассматривать как следствие двойной инверсии конфигурации. [3]
Если па - pa - положение исходного амина свободно ( Н Н) или занято группой R NO2 CC H, 5Оз Н, при атаке хлорид-иона происходит нуклеофильное замещение атомом хлора с образованием соединения ( 71); если оно занято группой RAlk, OAlk, NAlk2, замещение на хлор не происходит. [4]
Хотя механизм этих реакций во всех деталях не установлен, можно с достаточным основанием полагать, что первая стадия представляет собой образование неустойчивого смешанного ангидрида VIII, который далее смыкается, причем происходит атака хлорид-иона по углеродному атому карбонильной группы. Аналогичный механизм имеет место при образовании алкилхлоридов из спиртов и хлористого тионила ( стр. [5]
Хотя механизм этих реакций во всех деталях не установлен, можно с достаточным основанием полагать, что первая стадия представляет собой образование неустойчивого смешанного ангидрида VIII, который далее смыкается, причем происходит атака хлорид-иона по углеродному атому карбонильной группы. Аналогичный механизм имеет место при образовании алкилхлоридов из спиртов и хлористого тионила ( разд. [6]
Нуклеофил атакует этот катион по двум возможным положениям. Атака хлорид-иона на атом углерода, связанный с гидроксилышй группой, приводит к исходному соединению. [7]
Конечно, и в эта реакция может протекать с промежуточным образованием циклического галогениевого иона. Однако, если бы такой ион был симметричным, то по стерическим причинам он должен был бы раскрываться при атаке хлорид-иона по более доступному атому Ср а в качестве конечного продукта следовало бы ожидать образования 2-иод - 2-метил - 1 -хл орпропана. [8]
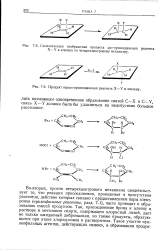 |
Схематическое изображение процесса ис-присоединения реагента X-Y к этилену по четырехцентровому механизму.| Продукт трдас-присоединения реагента X-Y к этилену. [9] |
Во-вторых, против четырехцентрового механизма свидетельствует то, что реакция присоединения, проводимая в присутствии реагентов, действие которых связано с предоставлением пары электронов ( нуклеофильные реагенты, разд. Так, присоединение брома к алкену в растворе в метиловом спирте, содержащем хлористый литий, дает не только ожидаемый дибромалкан, но также продукты, образующиеся при атаке хлорид-ионов и растворителя. [10]
Во-вторых, против четырехцентрового механизма свидетельствует то, что реакция присоединения, проводимая в присутствии реагентов, действие которых связано с предоставлением пары электронов ( нуклеофилъные реагенты, стр. Так, присоединение брома к алкену в растворе в метиловом спирте, содержащем хлористый литий, дает не только ожидаемый дибромалкан, но также продукты, образующиеся при атаке хлорид-ионов и растворителя. Такое участие нуклеофильных агентов, действующих извне, в образовании продуктов реакции служит серьезным доводом против одностадийного механизма. [11]
Страницы: 1