Коэффициент - диссоциация
Cтраница 3
Для определения коэффициента диссоциации электролита воспользуемся формулой (14.7), в которую входит эта величина. [31]
Пусть в каждой единице объема раствора имеется п молекул растворенного вещества, из которых an диссоциированы, а ( I - а п не диссоциированы. Коэффициент а называется коэффициентом диссоциации ] он показывает, какая доля всех молекул распалась на ионы. [32]
Пусть в каждой единице объема раствора имеется п молекул растворенного вещества, из которых an диссоциированы, а ( 1-а) п не диссоциированы. Коэффициент а называется коэффициентом диссоциации, он показывает, какая доля всех молекул распалась на ионы. [33]
Пусть в каждом см раствора имеется п молекул растворенного вещества, из которых an диссоциированы, а ( 1 - а) я не диссоциированы. Коэффициент а называется коэффициентом диссоциации; он показывает, какая доля всех молекул распалась на ионы. [34]
При небольшой концентрации раствора коэффициент диссоциации [ см. (32.9) ] является величиной постоянной, сумма подвижностей ионов Ь) Ъ ( - также приблизительно постоянна. [35]
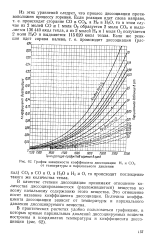 |
График зависимости коэффицента диссоциации Н2 и СО2 от температуры и парциального давления. [36] |
В качестве степени диссоциации принимают отношение количества диссоциировавшегося ( разложившегося) вещества ко всему начальному содержанию этого вещества. Это отношение носит название коэффициента диссоциации. Величина коэффициента диссоциации зависит от температуры и парциального давления диссоциируемого вещества. [37]
Отношение продиссоциированного количества СО2 или Н2О к исходному ( до диссоциации) называется коэффициентом диссоциации Последний как для СО2, так и для Н2О возрастает с повышением температуры и парциального давления - концентрации их в газовой смеси. При одинаковой температуре и концентрации коэффициент диссоциации СО2 примерно в три раза больше чем у КО, так как молекула последней термически более устойчива, чем молекула углекислоты. [38]
При этом предполагалось, что на массообмен влияет реакция неионизированного уранилнитрата с растворителем на поверхности раздела и было применено уравнение ( 6), в котором концентрации, относящиеся к водной фазе, выражены как концентрации неионизированного растворенного вещества. Последние были затем заменены общими концентрациями уранилнитрата путем введения коэффициента диссоциации. Конечное выражение показывает, что массо-иередача от водной фазы к растворителю является реакцией псевдо-третьего порядка, в то время как обратная реакция - первого порядка. [39]
В § 55 мы уже говорили, что сопротивление электролитов при нагревании уменьшается, т.е. электролиты имеют отрицательный температурный коэффициент сопротивления. Это происходит по двум причинам: во-первых, при увеличении температуры увеличивается коэффициент диссоциации а; во-вторых, при нагревании вязкость жидкостей уменьшается и поэтому подвижность ионов увеличивается. [40]
Зависимость р от концентрации раствора имеет сложный характер. При дальнейшем увеличении концентрации р достигает минимума, а затем возрастает вследствие убывания как коэффициента диссоциации а, так и подвижности ионов. [41]
Этот процесс называется молнзацией или рекомбинацией. Пусть RQ - концентрация молекул растворенного вещества, из которых сод диссоциированы на ионы, где а - коэффициент диссоциации. [42]
Диссоциация молекул на ионы оказывает влияние и на осмотическое давление, так как увеличивает число частиц в растворе. Увеличение числа частиц вызывает, при той же исходной концентрации, увеличение осмотического давления, измеряя которое можно определить коэффициент диссоциации, или изотонический коэффициент, как его назвал Вант-Гофф. [43]
Диссоциация молекул на ионы оказывает влияние и на осмотическое давление, так как увеличивает число частиц в растворе. Увеличение числа частиц вызывает, при той же исходной концентрации, увеличение осмотического давления, измеряя которое можно определить коэффициент диссоциации или изотонический коэффициент, как его назвал Вант-Гофф. [44]
В итоге подвижность ионов в растворах электролитов оказывается весьма небольшой, особенно в концентрированных растворах. Ввиду отсутствия законченной теории величины bi и Й2, входящие в формулу (8.61), берутся по данным экспериментов, как и константа К в выражении (8.60) для коэффициента диссоциации. [45]
Страницы: 1 2 3 4