Коэффициент - диффузия - ион - водород
Cтраница 1
Коэффициент диффузии ионов водорода приблизительно в четыре раза выше коэффициента диффузии кислорода, а поэтому выведенное выше условие будет достигнуто в том случае, когда одному молю кислорода будут соответствовать два моля ионов водорода. [1]
Значения коэффициентов диффузии ионов водорода и атомов кислорода были заимствованы из литературных данных и не отличались большой точностью. [2]
А - константа, зависящая от величины коэффициентов диффузии ионов водорода и цинка. [3]
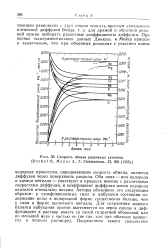 |
Скорость обмена различных катионов. [ Dicke. О., Meyer A., Z. Eiektrochem., 57, 905 ( 1953. ]. [4] |
Оба иона - ион водорода и катион металла - участвуют в процессе именно с различными скоростями диффузии, и коэффициент диффузии ионов водорода оказался аномально низким. [5]
В связи с малой растворимостью кислорода в водных средах, а также в связи с тем, что его коэффициент диффузии значительно меньше коэффициента диффузии ионов водорода, скорость коррозии с кислородной деполяризацией обычно лимитируется диффузией. На рис. 99 в упрощенном виде представлена типичная поляризационная диаграмма процесса коррозии с кислородной деполяризацией. [6]
Как видно из рис. 5, зависимость предельного тока от корня квадратного из скорости вращения медного электрода в 5 10 - 8МИ2804 с добавкой 0 2 М Na2S04 также выражается прямой. На основании полученных результатов вычислен коэффициент диффузии ионов водорода в 5 Ю-3 М H2S04 0 2 М Na2S04; он равен 2 0 10 6 смг / сек. То же значение для коэффициента диффузии получено и в других исследованных электролитах как с одно -, так и с двухвалентными катионами. [7]
 |
Упрощенная поляризационная диаграмма коррозии с кислородной деполяризацией. [8] |
Другим важным случаем электрохимического разрушения металлов является их коррозия с кислородной деполяризацией. В связи с малой растворимостью кислорода в водных средах, а также в связи с тем, что его коэффициент диффузии значительно меньше коэффициента диффузии ионов водорода, скорость коррозии с кислородной деполяризацией обычно лимитируется диффузией. На рис. 24.7 в упрощенном виде представлена типичная поляризационная диаграмма процесса коррозии с кислородной деполяризацией. [9]
Другим важным случаем электрохимического разрушения металлов является их коррозия с кислородной деполяризацией. В связи с малой растворимостью кислорода в водных средах, а также в связи с тем, что его коэффициент диффузии значительно меньше коэффициента диффузии ионов водорода, скорость коррозии с кислородной деполяризацией обычно определяется диффузией. На рис. 99 в упрощенном виде представлена типичная поляризационная диаграмма процесса коррозии с кислородной деполяризацией. [10]
 |
Упрощенная поляризационная диаграмма коррозии с кислородной деполяризацией. [11] |
Другим важным случаем электрохимического разрушения металлов является их коррозия с кислородной деполяризацией. В связи с малой растворимостью кислорода в водных средах, а также в связи с тем, что его коэффициент диф фузии значительно меньше коэффициента диффузии ионов водорода, скорость коррозии с кислородной деполяризацией обычно лимитируется диффузией. На рис. 24.7 в упрощенном виде представлена типичная поляризационная диаграмма процесса коррозии с кислородной деполяризацией. [12]
Это отвечает коррозии с водородной деполяризацией. Другим важным случаем электрохимического разрушения металлов является их коррозия с кислородной деполяризацией. В связи с малой растворимостью кислорода в водных средах, а также в - связи с тем, что его коэффициент диффузии значительно меньше коэффициента диффузии ионов водорода, скорость коррозии с кислородной деполяризацией обычно лимитируется диффузией. На рис. 103 в упрощенном виде представлена типичная поляризационная диаграмма продесса коррозии с кислородной деполяризацией. [13]
Скорость реакции ионного обмена исследована по объему ионов в системе ионит-раствор для различного времени контакта до установления равновесия. Исследованием установлено, что лимитирующей стадией процесса ионообмена является внутренняя диффузия. Установлено, что коэффициент диффузии ионов водорода в два раза выше чем у ионов калия. Повышенное значение коэффициента диффузии ионов водорода объясняется тем, что подвижность ионов водорода в 6 - 8 раз выше, чем у ионов калия. [14]
Скорость реакции ионного обмена исследована по объему ионов в системе ионит-раствор для различного времени контакта до установления равновесия. Исследованием установлено, что лимитирующей стадией процесса ионообмена является внутренняя диффузия. Установлено, что коэффициент диффузии ионов водорода в два раза выше чем у ионов калия. Повышенное значение коэффициента диффузии ионов водорода объясняется тем, что подвижность ионов водорода в 6 - 8 раз выше, чем у ионов калия. [15]
Страницы: 1