Коэффициент - диффузия - атом
Cтраница 1
Коэффициенты диффузии атомов Me к Mt зависят от состава окисла; работы разрыхления Q при диффузии атомов Me и Mt линейно зависят от концентрации атомов Me в решетке окисла. [1]
Коэффициенты диффузии атомов водорода и гелия определены по скорости проникновения этих газов из внешней среды. Диффузию лития можно проследить по изменению электропроводности, так как литий - донор электронов и изменяет электропроводность при ионизации. Вычисленное по уравнениям (6.3) и (6.5) значение D0 хорошо согласуется с экспериментально найденным. Во всех этих системах скорости диффузии значительны даже при низких температурах, что типично для диффузии по междоузлиям. [2]
Коэффициент диффузии атомов галлия в ртути равен 5 56 Ю - 5 см2 ( сек. [3]
Поскольку коэффициенты диффузии атомов различных элементов различны, скорость диффузии компонентов можно регулировать, используя легирующие элементы. [4]
Измерение коэффициентов диффузии атомов в газовой среде при высоких температурах представляет сравнительно сложную в экспериментальном отношении задачу. Этим можно объяснить тот факт, что до настоящего времени отсутствуют какие-либо справочные данные о коэффициентах диффузии атомов, за исключением ртути, диффузия которой изучалась при низких температурах. [5]
Измерения коэффициента диффузии атомов цинка в гелии при температуре 1740 К и давлении газа 1 атм дали величину 12 3 см2 / сек, что в 2 9 раза превышает соответствующий коэффициент диффузии атомов цинка в аргоне. Вычисления согласно формуле (47.5) дают разницу в коэффициентах диффузии атомов цинка в аргоне и гелии в 2 8 раза, что хорошо совпадает с экспериментом. [6]
Определим, следуя этой работе, коэффициент диффузии атомов С и найдем его зависимость от температуры, состава сплава и степени дальнего порядка. Для получения лишь качественных зависимостей расчет проведем в рамках обычно применяемой упрощенной модели, а именно, опять воспользуемся конфигурационной моделью парного взаимодействия соседних атомов, теорией диффузионных переходов Френкеля, примем, что кристаллическая решетка остается идеальной и не изменяется при изменении температуры, состава и порядка, не будем учитывать корреляцию в сплаве и квантовые особенности диффузии. [7]
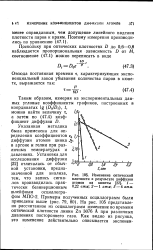 |
Изменение оптической плотности в результате диффузии атомов из кюветы. / - 0 22 атм. 2 - 1 атм. 3 - 4 атм. [8] |
Указанная методика была применена для определения коэффициентов диффузии атомов цинка в аргоне и гелии при различных температурах и 2 70 давлениях. [9]
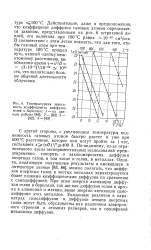 |
Температурная зависимость коэффициента диффузии 32 гелия в бериллии. / - по данным работы. 2 - . 3 - 7. 4 - J. [10] |
Действительно, даже в предположении, что коэффициент диффузии газовых атомов определяется законом, представленным на рис. 6 штриховой линией, его величина при 100 С равна - 10 - 50 см2 / сек. В соответствии с этим легко показать, что для того, чтобы газовый атом при температуре 100 С прошел путь, равный одному межатомному расстоянию, необходимо время % xiID - ( 3 - 10 - 8) 2 / 10 - 50 - 1035 сек, что значительно больше обычной длительности облучения. [11]
Больц-мана; Т - температура; D - коэффициент диффузии атомов; L - размер структурного элемента, относительно которого рассматривается диффузионно-вязкое течение. [12]
Энергия активации этого процесса равна 1 5 эВ, а коэффициент диффузии атомов кадмия составляет 10 - 6 см2 / с. При температурах, не превышающих 575 К, диффузия меди в CdS почти не наблюдается. [13]
При температуре выше 650 С коэффициент диффузии углерода становится больше коэффициента диффузии атомов металла. В результате этого более подвижные атомы углерода диффундируют в зону реакции и реагируют с окислителем. Скорость диффузии углерода в стали превышает скорость окисления металла. [14]
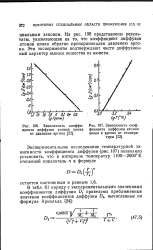 |
Зависимость коэффициента диффузии атомов цинка от давления аргона.| Зависимость коэффициента диффузии атомов цинка в аргоне от темпера-туры. [15] |
Страницы: 1 2 3