Коэффициент - кнудсеновская диффузия
Cтраница 2
Если газ диффундирует в поры, диаметр которых d /, то вместо / в формулу ( 128) входит d, и диффузия называется кнудсеновской. Коэффициент кнудсеновской диффузии DK в отличие от коэффициента молекулярной диффузии D, как очевидно из сказанного, не зависит от давления. Обычно DK D, этим главным образом объясняется уменьшение скорости диффузии в гранулах катализатора по сравнению со скоростью диффузии в газовой фазе. [16]
Превышение значений удельной поверхности, нестационарным методом, над значением, найденным стационарным методом, для того же образца порошка указывает на внутреннюю пористость частиц, однако не позволяет ее количественно измерить. В основу методов определения удельной поверхности дисперсных тел при кнудсеновском режиме течения положен коэффициент кнудсеновской диффузии D, теоретически найденный Б. В. Деряги-ным [59] для модели пористого тела или порошка ввидеиесоприка-непористых шаров. [17]
Низкие значения NS подразумевают, что адсорбция яда протекает медленно, и это в общем случае приводит к слабому влиянию ее на работу реактора. Таким образом, для низких значений модуля Тиле полезное время жизни ( пробег) реактора возрастает при уменьшении коэффициента кнудсеновской диффузии, в то время как при высоких значениях модуля Тиле верна обратная зависимость. [18]
 |
Зависимость эффективного коэффициента диффузии двуокиси азота от величины адсорбции. [19] |
На рис. 1 приведена зависимость коэффициентов De от величины адсорбции а. Так как исследуемый силикагель является мелкопористым, то нормальная диффузия исключается, и перенос адсорбата при не слишком высоких степенях заполнения должен осуществляться за счет кнуд-сеновской диффузии и миграции в адсорбированном слое. Эффективные коэффициенты диффузии De связаны с коэффициентами кнудсеновской диффузии Dk и коэффициентами поверхностной диффузии Da уравнением Дамкелера. Это свидетельствует о том, что адсорбированные молекулы сохраняют значительную свободу передвижения вдоль поверхности, и, следовательно, энергия специфического взаимодействия между молекулами адсорбата и свободными гидроксильными группами поверхности адсорбента [2] должна быть небольшой. [20]
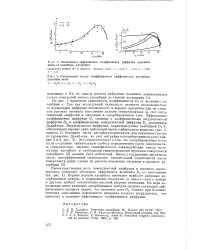 |
Зависимость эффективного коэффициента диффузии двуокиси азота от величины адсорбции. [21] |
На рис. 1 приведена зависимость коэффициентов De от величины адсорбции а. Так как исследуемый силикагель является мелкопористым, то нормальная диффузия исключается, и перенос адсорбата при не слишком высоких степенях заполнения должен осуществляться за счет кнуд-сеновской диффузии и миграции в адсорбированном слое. Эффективные коэффициенты диффузии De связаны с коэффициентами кнудсеновской диффузии Dk и коэффициентами поверхностной диффузии Zs уравнением Дамкелера. Это свидетельствует о том, что адсорбированные молекулы сохраняют значительную свободу передвижения вдоль поверхности, и, следовательно, энергия специфического взаимодействия между молекулами адсорбата и свободными гидроксильными группами поверхности адсорбента [2] должна быть небольшой. [22]
Для более быстрых реакций диффузия не успевает выравнивать состав реакционной смеси по глубине зерна катализатора. Процесс протекает в переходных кинетических режимах. Концентрация реагирующих веществ в глубине зерна становится ниже, а концентрация продуктов реакции выше, чем снаружи, в результате чего скорость реакции по глубине зерна уменьшается. В порах диаметром меньше средней длины свободного пробега молекул нормальная диффузия переходит в кнудсеновскую, а коэффициент кнудсеновской диффузии как известно снижается пропорционально уменьшению диаметра пор. Из однородных пористых структур для рассматриваемых реакций наиболее выгодна структура с капиллярами, диаметр которых равен средней длине свободного пробега молекул. С повышением давления длина свободного пробега уменьшается и становится выгодной более тонкопористая структура. [23]
Уилер изучил диффузию азота и окиси углерода друг в друга через катализаторы трех типов: активированный уголь, пористую глину и пористое стекло. Так как коэффициент кнудсеновской диффузии пе зависит от общего давления, а скорость обычной диффузии обратно пропорциональна давлению, то, изменяя давление, можно установить два типа диффузии. [24]
Поскольку теплопроводность твердого вещества катализаторов много выше теплопроводности газовых смесей, эффективные коэффициенты теплопроводности катализаторов обычно на порядок превышают коэффициент теплопроводности реакционной смеси. При проведении некоторых каталитических процессов с незначительными тепловыми эффектами, можно пренебречь существующими малыми температурными градиентами и рассматривать массопереноскак изотермический. В большинстве же случаев при анализе процессов переноса в катализаторах необходимо принимать во внимание существование заметных температурных градиентов. Так, например, различными исследователями экспериментально были получены следующие разности температур между внутренними и внешними зонами катализаторов: 17 5 - 37 4 С для реакции гидрогенизации этилена, 26 С для реакции диссоциации N2O, 40 - 60 С для реакции между водородом и кислородом, 6 - 27 С для реакции гидрогенизации бензена. Следовательно, при математическом описании процессов переноса, определяющих проведение экзотермических реакций с заметными скоростями, большими тепловыми эффектами и значительной энергией активации необходимо использовать уравнения связанного тепло - и массопереноса. Процесс переноса массы в пористых катализаторах анализировать значительно труднее, чем перенос теплоты. Это связано с тем, что помимо переноса за счет молекулярной диффузии в крупных порах имеет место кнудсеновский перенос в порах малого диаметра, причем оба типа переноса сопровождаются локальными адсорбционно-десорбционными процессами. Перенос массы в крупных порах, диаметр которых много больше длины свободного пробега молекул, хорошо описывается уравнением молекулярной диффузии. Массоперенос в порах, диаметр которых сравним с длиной свободного пробега молекул, определяется кнудсеновской диффузией. Разница между коэффициентами молекулярной и кнудсеновской диффузии может достигать двух порядков. Попытки вывести формулы для определения эффективных коэффициентов диффузии в пористых катализаторах на основе коэффициентов молекулярной и кнудсеновской диффузии с учетом распределения пор по диаметрам не привели к успеху, так как не удается учесть влияние извилистости пор и степень влияния непроточных пор на средний коэффициент переноса. [25]
Поскольку теплопроводность твердого вещества катализаторов много выше теплопроводности газовых смесей, эффективные коэффициенты теплопроводности катализаторов обычно на порядок превышают коэффициент теплопроводности реакционной смеси. При проведении некоторых каталитических процессов с незначительными тепловыми эффектами, можно пренебречь существующими малыми температурными градиентами и рассматривать массопереноскак изотермический. В большинстве же случаев при анализе процессов переноса в катализаторах необходимо принимать во внимание существование заметных температурных градиентов. Так, например, различными исследователями экспериментально были получены следующие разности температур между внутренними и внешними зонами катализаторов: 17 5 - 37 4 С для реакции гидрогенизации этилена, 26 С для реакции диссоциации N2O, 40 - 60 С для реакции между водородом и кислородом, 6 - 27 С для реакции гидрогенизации бензена. Следовательно, при математическом описании процессов переноса, определяющих проведение экзотермических реакций с заметными скоростями, большими тепловыми эффектами и значительной энергией активации необходимо использовать уравнения связанного тепло - и массопереноса. Процесс переноса массы в пористых катализаторах анализировать значительно труднее, чем перенос теплоты. Это связано с тем, что помимо переноса за счет молекулярной диффузии в крупных порах имеет место кнудсеновский перенос в порах малого диаметра, причем оба типа переноса сопровождаются локальными адсорбционно-десорбционными процессами. Перенос массы в крупных порах, диаметр которых много больше длины свободного пробега молекул, хорошо описывается уравнением молекулярной диффузии. Массоперенос в порах, диаметр которых сравним с длиной свободного пробега молекул, определяется кнудсеновской диффузией. Разница между коэффициентами молекулярной и кнудсеновской диффузии может достигать двух порядков. Попытки вывести формулы для определения эффективных коэффициентов диффузии в пористых катализаторах на основе коэффициентов молекулярной и кнудсеновской диффузии с учетом распределения пор по диаметрам не привели к успеху, так как не удается учесть влияние извилистости пор и степень влияния непроточных пор на средний коэффициент переноса. [26]
Страницы: 1 2