Коэффициент - массопере-дача
Cтраница 3
Так, для систем хорошо растворимых газов ( Ма 1), например, аммиак-вода, коэффициент массопере-дачи почти не зависит от гидродинамических параметров жидкой фазы ( от Rex) и, следовательно, требуется подвергать турбулиза-ции, главным образом, газовую фазу. Наоборот, для систем трудно растворимых газов ( Ma sS 0 1), когда коэффициент абсорбции мало зависит от Ref, целесообразно повышать скорость жидкого потока. [31]
Ожижающий агент, как указано выше, приходит в равновесие с частицами на относительно коротком участке псевдоожиженного слоя. Вследствие этого при достаточной высоте слоя массообмен-ные аппараты ( подобно теплообменным) могут быть рассчитаны по материальному балансу без участия коэффициентов массопере-дачи. [32]
 |
Кинетика процесса в соответствии с законом действующих масс ( Р, Т - const. [33] |
Практически скорость процесса рассчитывается через константу скорости процесса k или на основе фактического выхода продукта. Если кинетическое уравнение ( основная формула скорости) процесса известно, то для количественной оценки интенсивности работы реакторов и для технологического расчета производственных процессов лучше пользоваться константой скорости процесса k, которая в гетерогенных процессах называется коэффициентом массопере-дачи. [34]
 |
Растворы полиоксадиазола в концентрированной серной кислоте. [35] |
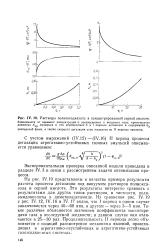
Эти результаты интересно сравнить с результатами для других типов растворов, в частности, поли-амидокислоты в диметилацетамиде. I период в одном случае заканчивается через 40 - 60 мин, в другом - через 3 - 5 мин. Такое различие объясняется значением коэффициента массопере-дачи газа в исследуемой жидкости; в данном случае они отличаются в 25 - 30 раз. Продолжительность II периода легко объясняется с позиций рассмотрения механизма явлений, происходящих в агрегативно-неустойчивых и агрегативно-устойчивых газожидкостных системах. [36]
Пассивной фазой является газовый поток, а активной - газ, находящийся в порах твердых частиц и сорбированный на активной поверхности. Соответственно, эффективная константа скорости межфазной диффузии т ] равна коэффициенту массопере-дачи р, умноженному на внешнюю поверхность единицы объема твердых частиц ае. Гидродинамический режим обеих фаз близок к идеальному вытеснению. [37]
Второй специфичной величиной является коэффициент массопере-дачи, который также меняется с изменением концентрации пузырьков. Естественно, что эта особенность должна каждый раз учитываться своим коэффициентом массопере-дачи К. Однако из-за отсутствия таких данных задача требует специального исследования. [38]
Основным фактором создания оптимального технологического режима и увеличения скорости процесса улавливания и переработки является температура. При абсорбции понижение температуры увеличивает движущую силу процесса, десорбция ускоряется при повышении температуры. Снижение диффузионного сопротивления на границе фаз и, соответственно, увеличение коэффициента массопере-дачи достигаются энергичным перемешиванием. Увеличению коэффициента массопередачи при переработке коксового газа способствуют также все методы, применяемые для создания развитой поверхности соприкосновения газа и жидкости ( см. гл. [39]
Из изложенного выше видно, что на процесс экстракции в распылительной колонне значительно влияет скорость движения диспергированной фазы. Скорость движения капель необходимо знать для расчета колонны. С одной стороны, ее величина требуется для определения времени контакта фаз и коэффициента массопере-дачи. [40]
Предложено математическое описание изотермического процесса противоточной абсорбции, осложненной необратимой химической реакцией второго порядка в жидкой фазе. Это описание учитывает режим работы и распределение концентраций по высоте аппарата. Принято, что: 1) диффузионное сопротивление в газовой фазе крайне мало; 2) продольное перемешивание газа и жидкости может быть описано с помощью диффузионной модели; 3) приведенные скорости газа и жидкости постоянны по высоте аппарата. Мгновенные значения коэффициентов массопере-дачи при хемосорбции представлены на основе пленочной теории. При рассмотрении бесконечно малого элемента абсорбера составлены его материальные балансы по общей концентрации компонента в газовой и жидкой фазах. Полученные системы дифференциальных уравнений решены для случая незначительного продольного перемешивания потоков. [41]
Эта система дифференциальных уравнений была численно проинтегрирована 66 при помощи большой электронно-счетной машины. Некоторые из полученных результатов представлены на рис. VI-8 - VI-11. Для сравнения приведены данные по реакции первого порядка и необратимой реакции второго порядка. На графиках по оси ординат отложены не коэффициенты массопере-дачи в условиях чисто физической абсорбции, а поправочные коэффициенты к ним. [42]
Эта система дифференциальных уравнений была численно проинтегрирована 6в при помощи большой электронно-счетной машины. Некоторые из полученных результатов представлены на рис. VI-8 - VI-11. Для сравнения приведены данные по реакции первого порядка и необратимой реакции второго порядка. На графиках по оси ординат отложены не коэффициенты массопере-дачи в условиях чисто физической абсорбции, а поправочные коэффициенты к ним. [43]
Эта система дифференциальных уравнений была численно проинтегрирована 6в при помощи большой электронно-счетной машины. Некоторые из полученных результатов представлены на рис. VI-8 - VI-11. Для сравнения приведены данные по реакции первого порядка и необратимой реакции второго порядка. На графиках по оси ординат отложены не коэффициенты массопере-дачи в условиях чисто физической абсорбции, а поправочные коэффициенты к ним. [44]
Эта система дифференциальных уравнений была численно прот интегрирована66 при помощи большой электронно-счетной машины. Некоторые из полученных результатов представлены на рис. VII-8 - VII-11. Для сравнения приведены данные по реакции первого порядка и необратимой реакции второго порядка. На графиках по оси ординат отложены не коэффициенты массопере-дачи в условиях чисто физической абсорбции, а поправочные коэффициенты к ним. [45]
Страницы: 1 2 3 4