Коэффициент - набухание - ионит
Cтраница 1
Коэффициент набухания ионитов в чистой воде в результате высокой гидрофильности ионогенных групп колеблется в пределах 1 4 - 5 и более. Так называемая поперечная сшивка ( как у полимеризационных ионитов) препятствует в значительной степени набуханию. [1]
Коэффициент набухания ионитов в обоих случаях заметно снижается по мере нагревания геля. [2]
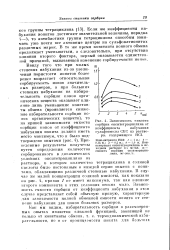 |
Зависимость емкости сорбции окситетрациклина от коэффициента набухания. [3] |
Если же коэффициенты набухания ионитов достигают значительной величины, порядка 4 - 5, то антибиотики группы тетрациклина способны занимать уже почти все активные центры на сульфокатионитах различных марок. В то же время константа ионного обмена продолжает уменьшаться, а следовательно, при отсутствии влияния второго фактора, первый оказывается единстрен-ной причиной, вызывающей изменение сорбируомости ионон. [4]
Возможно, что коэффициенты набухания ионитов при нагревании их при 160 - 180 понижаются в результате вторичных процессов при участии звеньев, сохранивших сульфогруппы, и десуль-фированных звеньев с образованием связи углерод - углерод между ядрами, принадлежащими различным цепям. [5]
Интересно отметить, что изменения коэффициента набухания ионитов 2а - Оа, синтезированных при комнатной температуре, не соответствуют понижению их обменной емкости и значения А ц колеблются в пределах 2.9 - 3.5. Более высокие значения Ан ионитов 5а и 6а ( соответственно 3.21, и 3.49) авторы объясняют тем, что при низкой температуре и большом избытке формальдегида степень поликонденсации не особенно велика. [6]
Показано, что при ионообменной сорбции больших органических ионов тетрациклина уменьшение количества сшивающего агента в ионите или увеличение коэффициента набухания ионита способствует возникновению пленочной кинетики. [7]
Представленные на рис. 59, 60 зависимости демонстрируют существенное уменьшение константы ионного обмена как для хлортетрациклина, так и для окситетрациклина в случае увеличения коэффициентов набухания ионитов. [8]
Из полученных экспериментальных данных можно сделать заключение, что при сорбции больших органических ионов ( таких как тетрациклин) возникновению пленочной кинетики способствует уменьшение количества сшивающего агента в ионите или увеличение коэффициента набухания ионита. Когда же часть активных центров ионита становится занятой ионами тетрациклина, и диффузия ионов в зерне ионита ухудшается, самой медленной стадией процесса ионообменной сорбции становится диффузия ионов тетрациклина внутри зерна ионита, и влияние пленки вокруг зерна ионита становится ничтожным. [9]
Как было указано выше, согласно [228], нагревание ионита КУ-1 в щелочном растворе ( например в 10 % - й Na2C03 при 90 в течение 4 час. Эти опыты не находят подтверждения в проведенных для сульфо-фенолформальдегидных ионитов исследованиях [9, 117] ( табл. 11.34); с повышением содержания сульфогрупп повышался коэффициент набухания ионитов, и только в немногих опытах этот показатель сохранялся примерно таким же. Возможность образования сульфогрупп за счет неактивной серы заставляет предполагать, что последняя может содержаться не только в суль-фоновых, но также в иных группах, например в сульфоэфир-ных. [10]
Это явление описано с помощью ряда моделей, как связанных, так и не связанных с представлением о давлении набухания. Важным фактором здесь является сжатие ионита при сорбции ионов органического вещества, что соответствует дегидратации и уменьшению абсолютной величины отрицательного значения термодинамического потенциала, которая обычно возрастает с увеличением коэффициента набухания ионита. [11]
Способность ионита к набуханию характеризуется коэффициентом набухания & Наб, равным отношению объема зерна ионита в данном растворе ( или в растворителе) к его объему в сухом состоянии. Систематических сведений о коэффициентах набухания ионитов не имеется. [12]
Страницы: 1