Диаграмма - состояние - даюта
Cтраница 1
Диаграммы состояния дают представление об условиях и последовательности минералообразования в исследуемых системах, позволяют сделать заключение о характере реакций, ведущих к образованию интересующих соединений. Поэтому изучение диаграмм состояния является необходимой теоретической основой процессов синтеза. Фторсиликатные системы, в которых при определенных условиях могут образоваться фазы фторамфиболового состава, изучены недостаточно. Это обусловлено прежде всего экспериментальными трудностями: сложным химическим составом, агрессивностью и склонностью к гидролизу оксифторидных систем, а также присутствием летучего компонента - фтора. [1]
Диаграммы состояния дают возможность, как это ясно из изложенного выше, выявить наличие химических соединений в системе, состав этих соединений, их способность к диссоциации при плавлении. Все эти данные оказывается возможным получить на основании анализа кривых, описывающих зависимость температуры появления новой фазы от состава системы. Изучение графиков, описывающих зависимость какого-либо физического свойства системы от ее состава, является задачей физико-химического анализа. В настоящее время физико-химический анализ широко используется для исследования не только однородных растворов, но и сложных многокомпонентных многофазных систем. [2]
Диаграммы состояния дают в сжатой и наглядной форме картину изменения строения и свойств сплава при изменении его концентрации и температуры, позволяют определить температуры плавления, затвердевания и аллотропических превращений в сплавах, изучить происхождение структур, наблюдаемых под микроскопом, и увязать структуру сплава с его механическими, технологическими и физико-химическими свойствами. При изыскании новых сплавов диаграммы позволяют заменить старый рецептурный метод новым научным методом, при помощи которого можно скорее и лучше подобрать их оптимальный состав. [3]
Диаграммы состояния дают наиболее ясное, представление о взаимодействиях между компонентами и новыми соединениями, твердыми и жидкими фазами и других процессах, имеющих место в силикатных системах. С помощью диаграмм определяют химический состав отдельных фаз, температуры начала и завершения процессов плавления и кристаллизации, изменение соотношения между жидкими и твердыми фазами. [4]
Диаграммы состояния дают в сжатой и наглядной форме картину изменения строения и свойств сплава при изменении его концентрации и температуры, позволяют определить критические точки плавления, затвердевания и аллотропических превращений в сплавах, дают возможность изучить происхождение структур, наблюдаемых под микроскопом, и увязать структуру сплава с его механическими, технологическими и физико-химическими свойствами. При изыскании новых сплавов диаграммы позволяют заменить старый рецептурный метод новым, научным методом, позволяющим гораздо скорее и лучше подобрать их оптимальный состав. [5]
Диаграммы состояния дают возможность, как это ясно из изложенного выше, выявить наличие химических соединений в системе, состав этих соединений, их способность к диссоциации при плавлении. Все эти данные оказывается возможным получить на основании анализа кривых, описывающих зависимость температуры появления новой фазы от состава системы. Изучение графиков, описывающих зависимость какого-либо физического свойства системы от ее состава, является задачей физико-химического анализа. [6]
Диаграммы состояния дают ответ на вопрос, из скольких и каких фаз состоит система данного состава при данных условиях. Точки на диаграмме, описывающие общий состав и условия существования системы, называются фигуративными точками. Зная число компонентов и определив число фаз по диаграмме, мы можем рассчитать по формуле Гиббса ( 36) число степеней свободы, которое является весьма важной физико-химической характеристикой системы. [7]
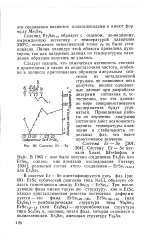 |
Система Er - Se. [8] |
Проведенные работы по изучению диаграмм состояния дают возможность оценить температуры плавления и стабильность отдельных фаз, что имеет практическое значение. [9]
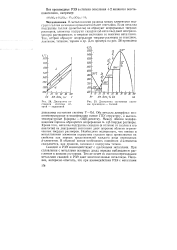 |
Диаграмма состояния системы иттрий - гадолиний.| Диаграмма состояния системы празеодим - галлий. [10] |
Оба металла диморфны: низкотемпературные - модификации имеют ГПУ-структуру, а высокотемпературные р-формы - ОЦК-решетку. Между обеими модификациями порознь образуются непрерывные а - и - твердые растворы. Кроме того, металлы подгруппы скандия ( в отличие от галлия и его аналогов) на диаграммах состояния дают широкие области ограниченных твердых растворов. Необходимо подчеркнуть, что именно в металлохимии элементов подгруппы скандия ярко проявляются их свойства как первых представителей каждого ряда переходных d - элементов. В обычной химии особенность поведения с / - элементов сказывается, как правило, начиная с подгруппы титана. [11]
 |
Диаграмма состояния системы празеодим - гашшй. [12] |
В металлохимии отличия между элементами подгрупп галлия и скандия проявляются более отчетливо. Если металлы подгруппы галлия ( sp - металлы) не образуют непрерывных твердых растворов, элементы подгруппы скандия дают неограниченную растворимость в твердом состоянии со многими металлами. Так, иттрий образует непрерывные твердые растворы со скандием, лантаном, титаном, торием, гадолинием и др. Кроме того, металлы подгруппы скандия ( в отличие от галлия и его аналогов) на диаграммах состояния дают широкие области ограниченных твердых растворов. Необходимо подчеркнуть, что именно в металлохимии элементов подгруппы скандия ярко проявляются их свойства как первых представителей каждого ряда переходных rf - элементов. В обычной химии особенность поведения d - элементов сказывается, как правило, начиная с подгруппы титана. [13]
 |
Диаграмма состояния системы празеодим - галлий. [14] |
В металлохимии отличия между элементами подгрупп галлия и скандия проявляются более отчетливо. Если металлы подгруппы галлия ( s / ьметаллы) не образуют непрерывных твердых растворов, элементы подгруппы скандия дают неограниченную растворимость в твердом состоянии со многими металлами. Так, иттрий образует непрерывные твердые растворы со скандием, лантаном, титаном, торием, гадолинием и др. Кроме того, металлы подгруппы скандия ( в отличие от галлия и его аналогов) на диаграммах состояния дают широкие области ограниченных твердых растворов. Необходимо подчеркнуть, что именно в металлохимии элементов подгруппы скандия ярко проявляются их свойства как первых представителей каждого ряда переходных rf - элементов. В обычной химии особенность поведения d - элементов сказывается, как правило, начиная с подгруппы титана. [15]
Страницы: 1