Коэффициент - распределение - железо
Cтраница 1
Коэффициент распределения железа возрастает с увеличением рН водной фазы; при рН 2 5 водная фаза практически не содержит железа. [1]
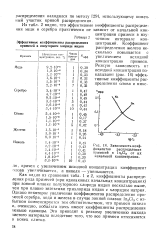 |
Зависимость коэффициентов распределения примесей в 1п2С13 от их начальной концентрации. [2] |
Коэффициент распределения железа несколько повышается с увеличением исходной концентрации примеси. [3]
FLO коэффициент распределения железа, начиная с определенной концентрации его в растворе, при дальнейшем уменьшении ее начинает падать, стремясь к нулю. [4]
Методика определения коэффициента распределения железа аналогична предыдущей. [5]
Однако, поскольку коэффициент распределения железа при экстракции диизобутил сульфидом приблизительно на 4 порядка меньше, чем при экстракции эфирами, и даже при высокой концентрации НС1 не превышает 0 01, этот способ не вызвал интереса. [6]
 |
Состав серии растворов ( в мл с постоянной ионной силой. [7] |
Далее рассчитывают отношение Da / D, где Z) 0 - коэффициент распределения железа в 1 М хлорной кислоте. [8]
Интересно поведение железа при поглощении катио-нитом из растворов соляной кислоты. Коэффициент распределения железа первоначально уменьшается с ростом молярности НС1, а затем снова возрастает, хотя известно, что в концентрированных растворах соляной кислоты железо находится в виде устойчивого отрицательного хлорид-ного комплекса. [9]
Как и при извлечении из хлоридных растворов, экстракция обычно растет с ростом концентрации НВг, но затем, в зависимости от природы растворителя, может уменьшаться, пройдя через максимум. При использовании ДЭЭ коэффициенты распределения железа растут с ростом его концентрации в области относительно высоких концентраций), что обусловлено процессами агрегации в органической фазе. Введение в водную фазу бромидов неэкстрагирующихся металлов способствует экстракции железа. [10]
Гексон следует предпочесть эфирам, потому что коэффициент распределения железа ( III) при экстракции гексоном значительно больше, чем при экстракции эфирами, и меньше зависит от концентрации кислоты. Кроме того, эфиры легче воспламеняются. [11]
Гексон следует предпочесть эфирам, потому что коэффициент распределения железа ( III) при экстракции гексоном значительно больше, чем при экстракции эфирами, и меньше зависит от концентрации кислоты. Кроме того, эфиры легче воспламеняются. [12]
Одним из путей эффективного повышения коэффициента распределения аналитической формы элемента является подбор растворителя-экстрагента. Так, при замене диэтилового эфира на метилизобутилкетон коэффициент распределения железа ( III) из солянокислого раствора возрастает более чем на порядок. При этом имеется в виду, что для водной фазы должны быть подобраны такие условия, при которых определяемый элемент максимально связан в аналитическую форму. При образовании комплексного соединения наиболее важен правильный выбор рН водного раствора. Механический перенос условий определения из справочников на конкретную систему часто приводит к ошибкам. Немаловажную роль также играет химическая природа вещества матрицы. [13]
Диссоциация в органической фазе возможна для соединений ионного характера при использовании растворителей с относительно высокой диэлектрической проницаемостью. Метилгексилкетона инертными в экстракционном отношении растворителями с различной диэлектрической проницаемостью, добивались либо уменьшения, либо увеличения коэффициентов распределения железа при экстракции его из солянокислых растворов. [14]
Имеется большой экспериментальный материал об экстракции железа ( III) различными растворителями из растворов хлоридов металлов в присутствии относительно больших количеств соляной кислоты. При замене НС1 на LiCl и при использовании не очень эффективных экстрагентов ( простые и сложные эфиры) коэффициенты распределения железа несколько снижаются. Из растворов А1С13 она бывает более высокой. [15]
Страницы: 1 2