Коэффициент - распределение - зависенок
Cтраница 1
Коэффициенты распределения зависят от температуры, поэтому некоторые разделения можно значительно улучшить в результате изменения температуры. Как было показано в работе / 11 /, в адсорбционных системах происходят и другие, более тонкие явления, которые могут обеспечить улучшенную селективность. [1]
Количественные значения коэффициентов распределения зависят от температуры, при которой производится экстракция, и от концентрации растворенного вещества. [2]
Хотя способность смолы к захвату катионов и коэффициенты распределения зависят от аниона соли, полимер с 18-краун-кольцом ( т 1) избирательно поглощает К и Cs, а полимер с 24-краун-кольцом ( т 2) - Rb и Cs, и, таким образом, происходит разделение ионов. [3]
Эта формула учитывает то обстоятельство, что коэффициенты распределения зависят от величины заряда иона и, соответственно, от степени закомплексованности данного иона. [4]
Можно заметить, что, когда концентрация железа в органической фазе достаточно высока и образуются ионные квад-риплеты, значения коэффициентов распределения зависят от концентрации, увеличиваясь с ростом концентрации железа. Мейер и Мецлер [210, 228] экспериментально подтвердили это толкование с помощью изопиестического и других методов. [5]
Измерены коэффициенты распределения смесей ме-тилциклогексанонов и метилциклогевсанолов между метилциклогексаном и гводой. Коэффициенты распределения зависят от концентрации веществ: для кетонов с ростом концентрации они увеличиваются, а для спиртов - уменьшаются. [6]
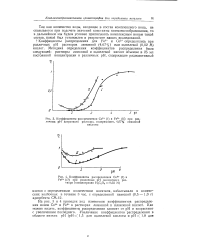
На рис. 3 и 4 приведен ход изменения коэффициентов распределения ионов Со2 и Fe2 в растворах лимонной и щавелевой кислот. Как можно видеть, коэффициенты распределения зависят от рН и возрастают с увеличением последнего. [8]
Приведенный вывод справедлив только в случае постоянного коэффициента распределения, не зависящего от концентрации экстрагируемого соединения. В общем случае этот вывод нельзя распространять на системы с переменным коэффициентом распределения, так как даже если С2г 7гСн то qi qC2 / Ci, так как концентрации C2i и Си не равны концентрациям С2 и GI, а коэффициенты распределения зависят от концентраций. [9]
Измерены коэффициенты распределения смесей метилцик-логексанонов и метилциклогексаиолов между метилциклогек-саном и водой. Обе системы ( метилциклогексан-кетоны-вода и метилциклогексан-спирты-вода) подчиняются законам разбавленных растворов. Коэффициенты распределения зависят от концентрации веществ: для кетонов с ростом концентра-дии они увеличиваются, а для спиртов - уменьшаются. [10]
Комплексообразование в водном растворе решающим образом влияет на экстракцию. В известном смысле правильным будет утверждение, что экстракция галогенидных комплексов определяется состоянием металла в водной фазе. Коэффициенты распределения зависят от степени образования комплексной формы, которая экстрагируется лучше других форм, что в свою очере. На экстракции сильно сказывается наличие или отсутствие процессов гидролиза и полимеризации. В связи с этим для понимания механизма экстракции галогенидных комплексов необходимо широко использовать достижения координационной химии. [11]
С) / С2 ( С - С2), где Сг и С2 - реальные концентрации в каждой фазе; С и С - фиктивные; / d и / С2 - коэффициенты массопередачи. Если эти коэффициенты равны и не зависят от концентрации, то Ki / K. Очевидно, что если коэффициенты распределения зависят от концентрации, то отношение коэффициентов массопередачи не может быть равно коэффициенту распределения. [12]
С и С - фиктивные; / Ci и / С2 - коэффициенты массо-лередачи. Если эти коэффициенты равны и не зависят от концентрации, то / С1 / / С27 - Очевидно, что если коэффициенты распределения зависят от концентрации, то отношение коэффициентов массопередачи не может быть равно коэффициенту распределения. [13]
Плутоний ( VI), подобно урану ( VI), экстрагируется гексоном значительно лучше остальных ионов плутония. Плутоний ( III) гексоном не экстрагируется, тогда как экстракция плутония ( IV) зависит от условий. ТБФ сравнительно хорошо экстрагирует плутоний ( IV) и плутоний ( VI), тогда как плутоний ( III) практически не экстрагируется. Следует подчеркнуть, что коэффициенты распределения зависят от точности соблюдения условий и поэтому значения их, приведенные в табл. 7.7, носят относительный характер. [14]
Самый старый метод фронтальной хроматографии обладает лишь немногими преимуществами. Лучшие результаты дает вытеснительная хроматография, однако наиболее эффективен метод проявительной хроматографии. Небольшое количество смеси ионов В и С, обладающих большим сродством к иониту, вводят в колонку вместе с ионами А, обладающими малым сродством к иониту. Величина вводимой пробьв пренебрежимо мала по сравнению с полным объемом колонки - Элюирование ведут ионами А. Коэффициент распределения - это отношение концентраций ионов в ионообменной фазе и в растворе, отнесенное к миллилитру раствора и к грамму ( сухой массы) или миллилитру ионообменной фазы. При слишком большом Ка, например более 30, хроматографические зоны расширяются и увеличивается время, необходимое для разделения. Степень сшивки ионитов должна быть достаточно высокой, чтобьь их объем оставался неизменным, или это должны быть макропористые иониты. Благоприятное действие оказывает увеличение скорости потока элюента в колонке, способствующее более равномерному распределению пленки жидкости по поверхности зерен ионита, но слишком сильное увеличение скорости может увести систему из оптимального равновесного состояния. Величины коэффициентов распределения зависят от состава элюента, и их можно регулировать в значительных пределах, добавляя комплексообразующие компоненты; например, при разделении лантанидов с этой целью используют органические оксикислоты. [15]
Страницы: 1