Коэффициент - распределение - иод
Cтраница 1
Коэффициент распределения иода между четырех-хлористым углеродом и водой, определенный при помощи иода-131, составляет 85 5 при 25 С. [1]
Предварительно находят коэффициент распределения иода между водой и органическим растворителем. [2]
Определив величину коэффициента распределения иода между водой и сероуглеродом при различных концентрациях Ja, Яковкин затем изучил распределение иода между водными растворами KJ и сероуглеродом. Полагая, что постоянное отношение, равное Красп. Ja в CSa и концентрацией свободных молекул Ja в воде а / и, Яковкин вычислил Кс по приведенному выше уравнению и нашел, что эта величина мало изменяется с изменением концентраций иода и йодистого калия. Таким же методом была изучена диссоциация КВгз, KBrJa, NaCUz и некоторых других комплексов. [3]
Определив величину коэффициента распределения иода между водой и сероуглеродом при различных концентрациях 12, Яковкин затем изучил распределение иода между водными растворами KI и сероуглеродом. Полагая, что постоянное отношение, равное Лрасп, устанавливается между полной концентрацией Ь в CS2 и концентрацией свободных молекул Ь в воде а / ц, Яковкин вычислил Кс по приведенному выше уравнению и нашел, что эта величина мало изменяется с изменением концентраций иода и йодистого калия. Таким же методом была изучена диссоциация КВг3, КВгЬ, NaClb и некоторых других комплексов. [4]
Определив величину коэффициента распределения иода между водой и сероуглеродом при различных концентрациях Ij, Яковкин затем изучил распределение иода между водными растворами KI и сероуглеродом. Полагая, что постоянное отношение, равное Лрасп, устанавливается между полной концентрацией г в CS2 и концентрацией свободных молекул Ь в воде a / и, Яковкин вычислил Кс по приведенному выше уравнению и нашел, что эта величина мало изменяется с изменением концентраций иода и йодистого калия. Таким же методом была изучена диссоциация КВгз, КВгЬ, NaClb и некоторых других комплексов. [5]
В работе следует определить коэффициент распределения иода между водой и органическим растворителем. [6]
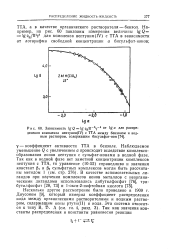 |
Зависимость lgQ lgqBar4Y - 4 от. а для РаспРе деления комплекса нептуния ( 1У с ТТА между бензолом и водным раствором, содержащим бисульфат-ион. [7] |
Несколько другое рассмотрение было проведено в 1909 г. Доусоном [9], который измерил коэффициент распределения иода между органическими растворителями и водным раствором, содержащим ионы ртути ( II) и иода. Эта система относится к типу В, 23, А ( см. гл. [8]
В присутствии хлористых солей, способствующих значительному повышению растворимости иода в воде, коэффициент распределения иода между органическими растворителями и водой снижается. [9]
Поэтому при изучении перехода иода из водного раствора в органический мы выбирали сначала систему иод - вода - н-гептан; коэффициент распределения иода в н-гептане немного ниже, чем в других подобных растворителях. К сожалению, профили, измеренные при переходе иода из органической в водную - фазу, были столь близки к исходным горизонтальным линиям ( см. рис. 2), что невозможно было точно измерить площади под кривыми. [10]
Производство иода десорбцией воздухом имеет ряд преимуществ по сравнению с угольным методом: возможность использования загрязненных и высокощелочных буровых вод, меньшая трудоемкость и простота автоматизации процесса, малый объем Рис - 65 Коэффициент распределения иода незавершенного производства; между ra30BOHHf 3 в - У раствор поэтому метод десорбции постепенно вытесняет угольный. [11]
В качестве проверки закона распределения рассмотрим данные для иода, растворенного в воде и четыреххло-ристом углероде. При промежуточных концентрациях коэффициент распределения иода между обеими фазами лежит в пределах этого интервала довольно близких значений. Таким образом, коэффициент распределения растворенного вещества между двумя растворителями остается в этом случае практически постоянным даже при высоких концентрациях. [12]
Это объясняется не только малой величиной коэффициента распределения иода, но и низкой концентрацией его в буровой воде. [13]
 |
Зависимость коэффициента распределения иода между газовой фазой и солевым раствором от концентрации солей ( по Стрельниковой52 при 25. [14] |
Процесс десорбции иода рассчитывается аналогично процессу десорбции брома. Так же как и для брома в присутствии хлористых солей, коэффициент распределения иода вследствие образования комплексного иона C1J2 снижается, а в присутствии сернокислых солей - повышается. [15]
Страницы: 1 2