Коэффициент - распределение - скандий
Cтраница 1
 |
Экстракция различных металлов из водных роданидных растворов этиловым эфиром. [1] |
Коэффициент распределения скандия не зависит от концентрации, он имеет одинаковое значение, как при первоначальной концентрации 20, так и при 1710 мг с2Оз на 100 мл раствора; на основании этого можно сделать заключение, что экстракция будет достаточно полной и при низкой концентрации скандия. [2]
Высокие значения коэффициентов распределения скандия были получены для подкисленных растворов тиоцианата. Как видно из данных, приведенных в табл. 5.25, в этих средах скандий можно отделить от кальция, лантана, самария и других элементов. [3]
В этом случае коэффициенты распределения скандия невелики, но избирательность экстракции неплохая, например, по отношению к редкоземельным элементам. [4]
Известен факт увеличения коэффициента распределения скандия при экстракции из смесей хлорной кислоты с азотной или соляной. [5]
Соотношение компонентов в комплексе, полученное при изучении зависимости коэффициента распределения скандия от равновесной концентрации роданид-иона и исходной концентрации коллидина ( Колл. [7]
От аниона кислоты и концентрации зависит в значительной мере и коэффициент распределения скандия. Он увеличивается с ростом кислотности. Более высокий коэффициент наблюдается при экстракции из азотнокислой среды по сравнению с хлоридными растворами [ 2, стр. [8]
Присутствие фосфорной кислоты ( даже в 2 М НС1О) резко понижает коэффициенты распределения скандия между КУ-2 и раствором ( табл.), что говорит об образовании в этих условиях фосфатных комплексов. [9]
Ранее было установлено [4], что влияние хлор-ионов до концентрации 3 г-ион / л на коэффициент распределения скандия весьма незначительно и им можно пренебречь. [10]
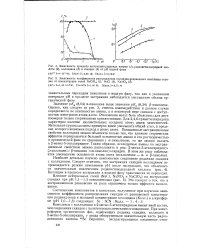
Хорошими высаливателями скандия являются также часто сопутствующие ему в сырье хлориды трехвалентного железа и алюминия, что видно из рис. 1, на котором приведены коэффициенты распределения скандия между ТБФ и слабокислыми ( рН 1 - 1 5) растворами хлоридов этих металлов. Для сравнения на этом же рисунке приведены данные по экстракции скандия из растворов соляной кислоты. Как видно, степень экстракции скандия из растворов хлорида трехвалентного железа приблизительно такая же, как из растворов соляной кислоты. [11]
Было изучено распределение скандия между его растворами в смеси минеральных кислот и ТБФ. Зависимость коэффициента распределения скандия от состава водной фазы во всех случаях имеет экстремальный характер. В системах НС1О4 - HN03 и НС1О4 - НС1 кривые имеют максимум, в системах HNO3 - НС1 и НС1О4 - Н2 SO4 - минимум. [12]
Было изучено распределение скандия между его растворами в смеси минеральных кислот и ТБФ. Зависимость коэффициента распределения скандия от состава водной фазы во всех случаях имеет экстремальный характер. В системах НС1О4 - HNO3 и НС1О4 - - НС1 кривые имеют максимум, в системах HNO3 - НС1 и НСЮ4 - H2SO4 - минимум. [13]
Переход железа в водную фазу при промывке незначительный. Наблюдаемое явление изменения коэффициента распределения скандия в присутствии РеС13 мы объясняем, как и ранее ( см. табл. 1), взаимодействием соединений скандия и железа в органической или водной фазах. Это обстоятельство позволяет применять для реэкстракции алюминия и двухвалентного железа растворы MgCl2 более низкой концентрации. [14]
Страницы: 1 2