Коэффициент - фугитивность
Cтраница 3
Точность коэффициентов фугитивности обеих фаз, установленных авторами работы [444] при помощи уравнений Соава и Пенга - Робинсона, одинакова. Пенг и Робинсон использовали предложенное ими уравнение для описания трехфазных смесей, содержащих воду, и изложили методику всех необходимых расчетов. Эти же ученые воспользовались разработанным ими уравнением для расчетов равновесия в многофазовых системах [549], например в смесях твердого и жидкого диоксида углерода и смесях воды с углеводородами. [31]
Сложность расчета коэффициента фугитивности чистого компонента заключается в том, что необходимо экстраполировать расчетные зависимости в гипотетическое состояние фазы, например при определении ff / P при температурах выше критической и давлениях ниже давления паров компонента и при определении f iV / P при давлении больше критического и температурах ниже критических. В связи с этим при определении фугитивности компонента в жидкости в диапазоне от рабочего давления до давления насыщенных паров жидкости при данной температуре подынтегральное выражение в уравнении (2.62) принимается постоянным. [32]
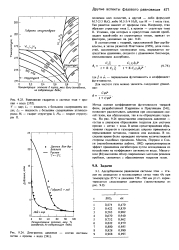 |
Равновесие гидратов в системе этан пропан вода.| Диаграмма давление - состав системы метан пропан вода. [33] |
Метод оценки коэффициентов фугитивности твердой фазы, разработанный Пэрришем и Праузницем [541], позволяет рассчитывать давления при диссоциации смесей газов, как образующих, так и не образующих гидраты. На рис. 9.24 представлена диаграмма давление - состав в диапазоне образования гидратов для системы пропан метан вода. В целях предотвращения образования гидратов в газопроводах широко применяется впрыскивание метанола, гликоля или аммиака. В последнее время было проведено изучение количественной стороны подобных процессов. Ментен, Пэрриш и Сло-ун ( неопубликованная работа, 1982) проанализировали эффект применения ингибиторов путем исследования их воздействия на коэффициент активности воды. Макогоном [84] выполнен обзор современных методов решения проблем, связанных с образованием гидратов газов. [34]
При низких давлениях коэффициент фугитивности Ф приближается к единице. При повышении давления коэффициент фугитивности значительно возрастает для тяжелых углеводородов и незначительно изменяется для легких газов. Значения коэффициента фугитивности паровой фазы определяются в зависимости от температуры, давления и состава паровой фазы. [35]
При низких давлениях коэффициент фугитивности Ф - паровой фазы близок к единице, с повышением же давления он заметно уменьшается для менее летучих компонентов, но для легких углеводородов меняется мало. Что касается коэффициента активности YJKJ, то с повышением концентрации компонента в смеси его значение приближается к единице. [36]
Для паровой фазы коэффициент фугитивности ( р, определяется из модификаций уравнения Редлиха - Квонга. [37]
В этой области коэффициент фугитивности и фактор сжимаемости примерно равны. [38]
При повышении давления коэффициент фугитивности значительно возрастает для тяжелых углеводородов и незначительно изменяется для легких газов. Значения коэффициента фугитивности паровой фазы определяются в зависимости от температуры, давления и состава паровой фазы. [39]
Для паровой фазы коэффициент фугитивности р, определяется из модификаций уравнения Редлиха - Квонга. [40]
Далее необходимо определить коэффициент фугитивности насыщенного пара PHIS. Для этого управление передается оператору с меткой 320, где приведенная температура сравнивается с коэффициентом, равным 0 56: Если приведенная температура TR 0 56, то для расчета давления насыщенного пара используется вириальное уравнение в форме разложения по давлению только до второго члена. [41]
Далее необходимо определить коэффициент фугитивности насыщенного пара PHIS. Если приведенная температура TR 0 56, то для расчета давления насыщенного пара используется вириальное уравнение в форме разложения по давлению только до второго члена. [42]
Если для расчета коэффициентов фугитивности в паровой фазе используется правило фугитивности Льюиса, то поправки Ft и F2 зависят от давления и температуры, но не зависят от у. Использование правила Льюиса приводит к математическим упрощениям, но, так как само по себе это правило мало пригодно, при наличии ЭВМ нет необходимости в его использовании. [43]
Изотермические отклонения энтропии и коэффициентов фугитивности, При расчете изотермических отклонений энтропии и коэффициентов фугитив-ности чистых газов или смесей, когда это возможно, необходимо следовать рекомендациям по расчету энтальпии, сделанным ранее. [44]
Коэффициент пропорциональности у называют коэффициентом фугитивности. [45]
Страницы: 1 2 3 4