Коэффициент - волновая функция
Cтраница 1
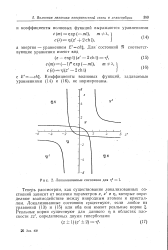 |
Локализованные состояния для т 2 1. [1] |
Коэффициенты волновых функций, задаваемые уравнениями ( 14) и ( 16), не нормированы. [2]
Определим коэффициенты волновой функции молекул. [3]
Определим коэффициенты волновой функции молекулы. [4]
Определим коэффициенты волновой функции молекул. [5]
Решим задачу о коэффициентах волновой функции (21.1) и энергии системы Нз при помощи вариационного метода. [6]
Решим задачу о коэффициентах волновой функции (26.1) и энергии системы Н2 при помощи вариационного метода. [7]
Решим задачу о коэффициентах волновой функции (21.1) и энергии системы Н2 при помощи вариационного метода. [8]
Для второго дублета (5.8) при этом могут быть найдены все коэффициенты волновых функций, поскольку из эксперимента определяются две величины, а благодаря соотношению нормировки из трех коэффициентов действительно неизвестными являются только два. [9]
Поля, квантование которых рассмотрено выше, яв - ляются эрмитовыми, так как коэффициенты волновых функций с положительной энергией и комплексно сопряженных им волновых функций представляют собой эрмитово сопряженные операторы. Можно рассмотреть те перь более общий случай, когда эти коэффициенты, будучи по-прежнему операторами рождения и уничтожения частиц, уже не являются эрмитово сопряженными друг другу. [10]
Последнее равенство означает, что наша волновая функция соответствует магнитному моменту, лежащему под углом а к оси г, и угол а, введенный для нормировки коэффициентов волновой функции, получает простую физическую интерпретацию. [11]
Речь идет о процессе с участием двух фо-нонов. Вычисление коэффициентов волновой функции и соответствующих вероятностей перехода мы предоставляем в качестве упражнения самому читателю. [12]
 |
Контурная диаграмма электронной плотности молекулы СО. [13] |
Определив вариационным методом коэффициенты волновой функции, построенной по методу ЛКАО, можно рассчитать распределение электронной плотности, и, построив контурную диаграмму, получить наглядное представление о распределении электронного заряда в молекуле и на отдельных орби-талях. [14]
Главная цель данного раздела состоит в том, чтобы показать, как величины параметров взаимодействия определяют природу адсорбированных частиц и способ возникновения компенсирующего заряда в кристалле. Для этого следует учесть два общих вывода, следующих из теории молекулярных орбит. Известно, во-первых, что если к идеальному кристаллу, содержащему N электронных уровней, приблизить водородоподобный инородный атом, то комбинированная система будет иметь N уровней, каждый из которых способен вместить два электрона. Во-вторых, сумма квадратов коэффициентов волновых функций с ( т) для всех N 1 уровней равна единице для всех атомов, включая и инородный атом. Если на каждом из N уровней находится по два электрона, то это значит, что инородный атом существует на поверхности как анион. Конечно, для того чтобы достигнуть заполнения каждого из имеющихся уровней двумя электронами, следует добавить в систему один избыточный электрон. Сказанное справедливо для кристалла полупроводника р-типа либо потому, что он содержит примеси, либо из-за его нестехиометричности. Число N должно, однако, включать только уровни нормальной зоны, но не дискретные уровни, лежащие непосредственно над ней и создающие полупроводниковую электропроводность р-типа в кристалле. Аналогичные соображения применимы и для полупроводников п-типа. [15]
Страницы: 1