Коэффициент - активность - соляная кислота
Cтраница 1
Коэффициенты активности соляной кислоты приведены в табл. 28 ( ем. [1]
Как видно, коэффициент активности соляной кислоты при малых концентрациях в этаноле более, чем в 200 раз превышает свое значение в воде при той же моляльности. Различие в коэффициентах активности для незаряженных молекул в разных растворителях обычно меньше, чем для ионных растворов. [2]
Допустим, требуется определить коэффициент активности соляной кислоты в растворах различной концентрации. [3]
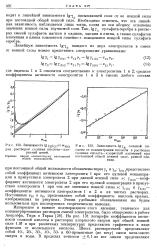 |
Зависимость IgfnTci от mHci [ IMAGE ] Зависимость. [4] |
На рис. 131 логарифм коэффициента активности соляной кислоты в растворах хлористого натрия при общей ионной силе 1 М и при различных температурах представлен графически в виде функции от моляльности кислоты. Шесть растворителей представляют собой 10 -, 20 -, 30 -, 40 -, 50 - и 60-процентные ( по весу) смеси метилового спирта и воды. [5]
Пусть, например, необходимо определить коэффициенты активности соляной кислоты при различных концентрациях. [6]
Бее величины в правой части этого уравнения известны, поскольку У TjiYci т С - коэффициент активности соляной кислоты при нулевой концентрации в растворах хлористого натрия ( табл. 161), был определен. [7]
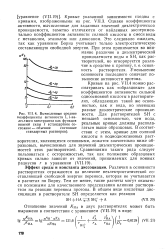 |
Вычисленные средние коэффициенты активности I, 1-ва-леьтного электролита как функция ионной силы / ( стандартное со. [8] |
Кривые указанной зависимости сходны с кривыми, изображенными на рис. VII.3. Однако коэффициенты активности, вычисленные для заданных значений диэлектрической проницаемости, заметно отличаются от найденных экспериментально коэффициентов активности соляной кислоты в смеси воды с метанолом, этанолом или диоксаном. Это следовало ожидать, так как уравнение Борна учитывает только электростатическую составляющую свободной энергии. Уменьшение основности последнего означает повышение активности протона. [9]
Так называемый эффект хлорида лития стал понятен, как только установили, что в концентрированных растворах эта соль обладает очень высоким коэффициентом активности. Аномальные результаты приписываются соляной кислоте, так как при высоких концентрациях коэффициенты активности соляной кислоты и хлорида лития очень близки. Остается неясным вопрос о том, почему сорбция металлов из растворов в соляной кислоте ненамного больше. По-видимому, причина этого кроется в ассоциации водорода и хлорид-ионов с образованием соляной кислоты. [10]
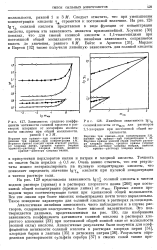 |
Зависимость среднего коэффициента активности соляной кислоты в растворах хлоридов от логарифма моляльности кислоты при общей моляльности. [11] |
Аналогичная линейная зависимость часто наблюдается и в случае растворов, содержащих электролиты с более высокой валентностью. Это подтверждается данными, представленными на рис. 130, где изображена зависимость коэффициента активности соляной кислоты в растворах хлористого алюминия [33] при постоянной общей ионной силе от моляльности ( ионной силы) кислоты. [12]
Эти данные свидетельствуют о том, что во многих случаях коэффициент активности больше в неводных средах, чем в водных. Сделанное заключение находит подтверждение также при оценке влияния органического растворителя ( эффект среды) на коэффициент активности соляной кислоты и других электролитов. На рис. VII.3 представлен средний коэффициент активности у соляной кислоты в воде и пяти неводных растворителях как функция моляльности кислоты. [13]
В нашем случае нужно знать величины средних коэффициентов активности НСЮ и HN03 в указанных выше тройных системах. Эта закономерность была проверена авторами для коэффициентов активности соляной кислоты в системе HClO - HCl-HjO и получила подтверадение в настоящей работе для хлорной и азотной кислот в исследованных растворах. [14]
Если, однако, в качестве макроэлектролита используется соляная кислота, положение существенным образом изменяется. Кривые, выражающие зависимость D от концентрации соляной кислоты, начинаются так же, как и соответствующие кривые для хлорида лития. Таким образом, кривая для соляной кислоты весьма необычна: она пересекает все другие кривые, и ее форму нельзя объяснить только изменением коэффициентов активности соляной кислоты в фазе раствора, поскольку они мало отличаются от коэффициентов активности хлорида лития. Как мы увидим ниже, эта особенность присуща не только соляной кислоте, но и другим кислотам, и поэтому ее можно назвать кислотным эффектом. Причины кислотного эффекта должны состоять в каких-то изменениях фазы ионита. [15]
Страницы: 1