Температурный коэффициент - подвижность
Cтраница 1
Температурный коэффициент подвижности l / 29i ( А / АУ) оказывается довольно большим ( - 0 02); при нагревании раствора на 1 С подвижность, а следовательно, и электропроводность возрастают примерно на 2 %, что приводит к необходимости применять термостаты для точного измерения электропроводности. Наибольший температурный коэффициент характерен для ионов с относительно малой подвижностью и наоборот. Наличие положительного температурного коэффициента подвижности ионов, по-видимому, объясняется уменьшением вязкости с температурой. [1]
Ниже приведены температурные коэффициенты подвижности и величины энергии А. [2]
В заключение следует заметить, что сопоставление температурных коэффициентов подвижности и вязкости является косвенным доказательством увеличения и уменьшения подвижности молекул воды вблизи иона по сравнению с подвижностью молекул воды в отсутствие ионов. [3]
В заключение следует заметить, что сопоставление температурных коэффициентов подвижности и вязкости, положенное Самойловым в основу представлений о гидратации, является косвенным доказательством увеличения и уменьшения подвижности молекул воды вблизи иона по сравнению с подвижностью молекул воды в отсутствии ионов. [4]
В заключение следует заметить, что сопоставление температурных коэффициентов подвижности и вязкости является косвенным доказательством увеличения и уменьшения подвижности молекул воды вблизи иона по сравнению с подвижностью молекул воды в отсутствие ионов. [5]
 |
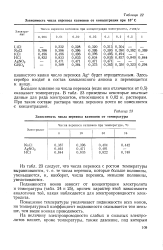
Зависимость числа переноса катионов от температуры.| Зависимость предельной ионной подвижности ( 10 См - м2 - моль 1 некоторых ионов от температуры при бесконечном разведении. [6] |
Повышение температуры увеличивает подвижность всех ионов, причем температурный коэффициент подвижности оказывается обычно тем меньше, чем выше ионная лроводимость. [7]
 |
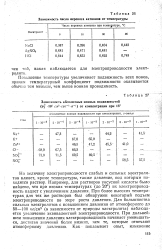
Зависимость числа переноса катионов от концентрации при 18 С.| Зависимость числа переноса катионов от температуры. [8] |
Повышение температуры увеличивает подвижности всех ионов, но температурный коэффициент подвижности оказывается тем меньше, чем выше ионная проводимость. [9]
 |
Зависимость числа переноса катионов от температуры. [10] |
Повышение температуры увеличивает подвижность всех ионов, причем температурный коэффициент подвижности оказывается обычно тем меньше, чем выше ионная проводимость. [11]
Аномальное поведение протона и соответственно гидроксил-иона проявляется и в некоторых других свойствах. Так, из значений температурного коэффициента подвижности этих ионов следует, что этот процесс в широкой области температур не может быть охарактеризован единой энергией активации. Эта особенность, отмеченная Нойесом [137] и Джонстоном [138], не является необычной для кинетики процессов, происходящих в воде, где структура растворителя меняется с температурой. Так, например, энергия активации текучести, молекулярной и ионной диффузии [139] и диэлектрической релаксации [91] в воде заметно зависит от температуры. [12]
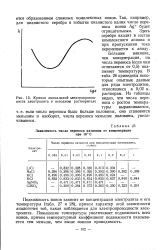 |
Кривая аномальной электропроводности электролита в неводном растворителе. [13] |
Подвижность ионов зависит от концентрации электролита и его температуры ( табл. 27 и 28), причем характер этой зависимости аналогичен той, какая наблюдается для электропроводности электролита. Повышение температуры увеличивает подвижность всех ионов, причем температурный коэффициент подвижности оказывается тем меньше, чем выше ионная проводимость. [14]
Предполагается, что процесс образования водорода - бимолекулярная реакция. При таком механизме образования водорода энергия активации не зависит от энергии связи С - Н и может рассматриваться как температурный коэффициент подвижности углеродных сеток. [15]
Страницы: 1