Температурный коэффициент - различная реакция
Cтраница 1
Температурные коэффициенты различных реакций могут значительно различаться. Однако в целом при снижении температуры алкилирования уменьшается скорость и повышается избирательность первичного алкилирования, что улучшает качество получаемого продукта. Сернокислотное алкилирование проводят при температуре от - 1 до 16; при более низких температурах кислота застывает, а при: более высоких - чрезмерно усиливаются реакции окисления. При фтористоводородном алкилиро-вании температурные пределы могут быть значительно шире; это и является одним из важнейших преимуществ фтористоводородного процесса. Вследствие экономических преимуществ, обусловленных возможностью отказа от применения холодильных систем, фтористоводородное алкилирование обычно проводят при минимальной температуре, достигаемой при водяном охлаждении, хотя дальнейшее снижение температуры реакции ( при соответствующем изменении некоторых других параметров процесса, в частности концентрации катализатора) позволяет значительно улучшить качество продукта. [1]
Повышение температуры неизменно сопровождается повышением скорости реакций над катализаторами крекинга, однако температурные коэффициенты различных реакций сильно различаются. Кажущиеся энергии активации изменяются в пределах 10 - 35 ккал / молъ. [2]
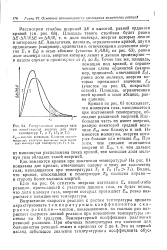 |
Распределение молекул газа НО кинетической энергии для двух. [3] |
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции - числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. [4]
 |
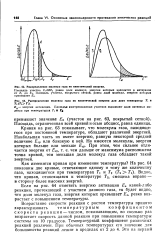
Распределение молекул газа по кинетической энергии.| Распределение молекул газа по кинетической энергии для двух температур Т и Г2 ( Г2Г. [5] |
Воз растание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции - числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. [6]
 |
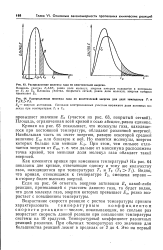
Распределение молекул газа по кинетической энергии.| Распределение молекул газа по кинетической энергии для двух температур Т, и. [7] |
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции - числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. [8]
 |
Распределение молекул газа по кинетической энергии.| Распределение молекул газа по кинетической анергии для двух температур Г, и. [9] |
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости р е а кци и - числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. [10]
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции - числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10 градусов. Температурный коэффициент различных реакций различен. [12]
Страницы: 1
