Молярный коэффициент
Cтраница 3
Интенсивность поглощения, измеряемая, например, значением молярного коэффициента е поглощения в максимуме полосы, зависит от вероятности данного электронного перехода. С этой точки зрения в спектроскопии различают разрешенные и запрещенные переходы. [31]
Определение ведут или по светопоглощению суспензии образующегося соединения с молярным коэффициентом ( е) равным 2.4 - 104, или по светопоглощению красителя, образующегося по реакции между оксином и диазотированной сульфаниловой кислотой, молярный коэффициент поглощения в пересчете на фосфор при этом равен 5 4 - 104 при 490 нм. [32]
Аналогичный характер зависимости от Нуд и Р получен и для молярного коэффициента экстинции этих соединений. [33]
Хорошим критерием деструкции нативной структуры ( разрыва водородных связей) служит молярный коэффициент экстинк-ции е ( Р) в ультрафиолетовой области спектра, где дезоксирибонуклеиновая кислота имеет широкий максимум поглощения в области 2580 - 2630 А. [34]
В данном случае свойством, зависящим от самой системы, является молярный коэффициент экс-тинкции раствора при выбранной длине волны ( уравнение ( III. Обсуждение отклонений от закона Бера - Ламберта выходит за рамки этой книги; читатель может прочесть о них в специальных пособиях по спектроскопии. [35]
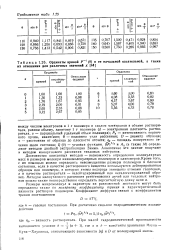 |
Ординаты кривой Р ( 6 и ее начальной касательной, а также их отношения для различных значений х. [36] |
Размеры макромолекул и параметры их равновесной жесткости могут быть определены также по молярному коэффициенту трения и характеристической вязкости растворов полимеров. [37]
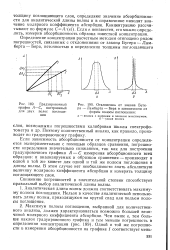 |
Градуировочный график А-С, построенный для двух полос поглощения.| Отклонения от закона Бугера - Ламберта - Бера в зависимости от формы полосы поглощения. [38] |
Максимум полосы поглощения, выбранной для количественного анализа, должен характеризоваться возможно большей величиной молярного коэффициента абсорбции. [39]
По атласу ультрафиолетовых спектров, не имея ни одного индивидуального углеводорода, нами были вычислены средние молярные коэффициенты. [40]
Все эти соединения хорошо экстрагируются хлороформом; измерены спектры поглощения хлороформных экстрактов комплексов и установлены их молярные коэффициенты светопогло-щення. При рН 5 - 6 образуются комплексы типа А; наиболее полно эти комплексы образуют более сильные основания - пиридин, хинолин и пирамидон. Более слабые основания - антипирин и диантипирилметан - лучше образуют соединения типа В, причем реакция идет в сильно кислой среде. [41]
Цифровые методы позволяют исправлять аппаратурные погрешности, вычислять оптические плотности и при наличии подходящих стандартов находить молярные коэффициенты эк-стинкции. [42]
Однако чаще всего не удается непосредственно использовать уравнение ( 3 - 4), поскольку величины молярных коэффициентов xt и 2 неизвестны. [43]
Так, молярный коэффициент погашения висмутового комплекса ди - [ 3-нафтилтиокарбазона ( Ег 170 000) больше молярного коэффициента такого же комплекса дифенилтиокарбазо-на ( Е % 45 000) в 3 7 раза. Это значит, что концентрация висмута в растворе может быть в 3 7 раза меньше при определении его с ди-р-нафтилтиокарбазоном, чем с дифенилтиокарба-зоном. [44]
 |
Оценка нижней границы определяемых содержаний и пределов обнаружения элементов в фотометрических методиках ( 37, Р 0 95. [45] |
Страницы: 1 2 3 4