Истинный коэффициент - перенос
Cтраница 1
Истинные коэффициенты переноса а и ( 1 - а) могут быть вычислены по уравнениям (64.13), если установлены лимитирующая стадия и стехиометрическое число. [1]
Истинные коэффициенты переноса а и ( 1 - а) могут быть найдены по уравнениям (64.13), если установлены лимитирующая стадия и стехиометрическое число. [2]
Истинные коэффициенты переноса а и ( 1 - а) могут быть вычислены по уравнениям (64.13), если установлены лимитирующая стадия и стехиометрическое число. [3]
Близость величины истинного коэффициента переноса и отношения AS / AS к 0 5 свидетельствует о сходной структуре растворителя, окружающего частицы в растворе и в переходном состоянии, которому отвечает заряд, промежуточный между зарядами исходного реагента и продукта реакции. [4]
Если в электрохимической стадии одновременно участвуют z электронов, то 3 fiz, где р - истинный коэффициент переноса анодного процесса. [5]
В таких случаях можно принять % х 70 и в первом приближении не учитывать специфическое взаимодействие электрохимически активного комплекса с электродом, что упрощает расчет истинного коэффициента переноса исходя из определяемых экспериментально кажущихся коэффициентов переноса. [6]
Здесь аа и ак - кажущиеся, или эффективные, коэффициенты переноса анодной и катодной реакции. Их связь с истинными коэффициентами переноса а и ак ( а ак 1; аа 0; ак 0) определяется механизмом реакций. [7]
Здесь аа и ок - кажущиеся, или эффективные, коэффициенты переноса анодной в катодной реакции. Их связь с истинными коэффициентами переноса аа и ак ( аа ак 1; аа 0; ак 0) определяется механизмом реакций. [8]
Предполагая, что значения истинных коэффициентов переноса аир близки к 0 5, приведенные выше данные можно рассматривать как свидетельство в пользу одновременного ( или практически одновременного) переноса двух электронов в электрохимической стадии. [9]
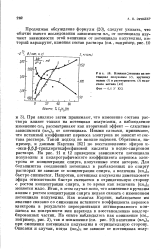 |
Влияние этанола на по-тенциал полуволны ( 1, крутизну волны ( 2 и растворимость ( 3 йодистого метила Фон - 0 1 N КС1. [10] |
При анализе затем принимают, что изменение состава раствора влияет только на потенциал полуволны, а наблюдаемое изменение апа рассматривают как вторичный эффект - следствие зависимости ( апа) п от потенциала. Иными словами, принимают, что истинный коэффициент переноса электрона не зависит от состава раствора. Такой подход не вполне надежен. [11]
Из уравнения (6.31) видно, что кажущийся коэффициент переноса можно рассчитать по экспериментальному значению Ь / г, не делая какого-либо предположения о числе электронов, участвующих в медленной электрохимической стадии. Если z электронов одновременно участвуют в электрохимической стадии, то a az, где а - - истинный коэффициент переноса катодного процесса. [12]
Если коэффициенты диффузии частиц О и R приблизительно равны, то результат вычисления ( &0) очень слабо зависит от о. Если для какого-либо изучаемого электролита известна зависимость q от Е, то, как это обычно делается, находят истинную стандартную константу скорости ( k0) и истинный коэффициент переноса. Для констант скоростей реакций первого порядка, не превышающих 10 - 2 см - с-1, особыми преимуществами при кинетических исследованиях обладает полярографический метод ввиду быстроты и легкости его применения. [13]
Поскольку ф изменяется вместе с концентрацией электролита и потенциалом электрода, величина ( i) зависит не только от концентрации, но и от потенциала, а величина ( &0) - не только от потенциала, но и от концентрации. Лишь в случае изменений ф на очень малую по сравнению с ri величину можно считать, что () приблизительно постоянно. Это приближение оправдано лишь в растворах сравнительно высокой ионной силы ( 1 М) и, далее, лишь в отсутствие многозарядных ионов в растворе, а также вдали от потенциала нулевого заряда. Если ( i) a принято постоянным, то даже если истинный коэффициент переноса и не будет иметь сколько-нибудь значительной зависимости от потенциала в исследуемой области, экспериментально определяемый коэффициент переноса будет зависеть от потенциала. [14]
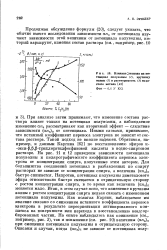 |
Влияние этанола на по-тенциал полуволны ( 1, крутизну волны ( 2 и растворимость ( 3 йодистого метила Фон - 0 1 N КС1. [15] |
Страницы: 1 2