Истинный коэффициент - распределение
Cтраница 1
Истинный коэффициент распределения ( отношение активностей) остается на всем протяжении постоянным; он равен 311 12 при 25 С. [1]
Рассчитаны истинные коэффициенты распределения незакомплексованного брома в растворах бромида и хлорида натрия. [2]
К - истинный коэффициент распределения; и и xt - доля поперечного сечения колонки, занятая газовой и жидкой фазами. [3]
Следует иметь в виду, что константа равновесия А, определяемая уравнением ( 21), и истинный коэффициент распределения К1 ( см. рис. 19) связаны множителями RT и 1 / ( 1 - - A2 [ H20 ]), причем последний множитель принят за постоянную величину. [4]
Определены брутто-коэффициентн молярного погашения брома и хлористого брома и константы образования комплексных ионов в растворах, рассчитаны истинные коэффициенты распределения незакомплексованных брома и хлористого брома. Рассмотрены процессы десорбции брома из растворов с учетом его комплексообразования и абсорбции брома из газовой фазы растворами аммиака и едкого натра. Приведены данные по упругости паров воды и брома над растворами бромида и хлорида железа. [5]
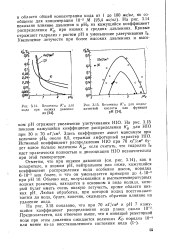 |
Величины К а для иода при низких давлениях.| Величины К. о для иодно. [6] |
Здесь коэффициент имеет максимум при величине рН0 около 8 5, отражая амфотерный характер НЮ. Истинный коэффициент распределения НЮ при 70 кГ / см2 будет вдвое больше величины K D, если считать, что гидролиз Ь идет практически полностью и диссоциация НЮ незначительна при этой температуре. [7]
Для каждого индивидуального вещества, если оно при переходе в другую фазу не диссоциирует и не образует ас-социатов, коэффициент распределения при постоянной температуре есть величина постоянная. Это так называемый истинный коэффициент распределения / С ст. Если вещество в растворителе может существовать в различных формах, например в виде ионов и молекул, то постоянство коэффициента распределения будет соблюдаться для каждой из форм существования вещества. [8]
Выведена теоретическая зависимость величин истинных коэффициентов распределения от различных параметров. [9]
Уран довольно хорошо растворим в церии ( 3 6 %) и, вероятно, в лантане. Коэффициент распределения осколочного церия, приведенный в первой половине табл. 40, не является истинным коэффициентом распределения, а выражает эффект изотопного разбавления, зависящий от сотношения объемов фаз. [10]
Для веществ, не меняющих форму своего существования в растворе, понятия истинного и видимого коэффициентов распределения совпадают. Для веществ, форма существования которых в растворе может меняться, постоянное значение при постоянной температуре сохраняет только истинный коэффициент распределения. Величина видимого коэффициента при постоянной температуре меняется с изменением факторов, влияющих на формы существования вещества. Например, для слабых электролитов таким фактором является рН, так как изменение реакции среды вызывает изменение степени диссоциации. [11]
Установлено, что относительная летучесть, или видимый коэффициент распределения аммиака, является функцией температуры концентрации и рН раствора, причем определяющим фактором является температура. Поскольку аммиак переходит из воды в пар в молекулярной форме, была дана поправка на ионизацию NH4OH в растворе и вычислен истинный коэффициент распределения аммиака. [12]
Приводимые во всех известных работах, например в [ I, 6, 7 ], значения коэффициентов распределения брома Нэ являются отношением концентраций брутто-брома в газовой фазе в его брутто-содеряанию в жидкой фазе. Поэтому для растворов хлоридов и бромидов величины Нд являются кажущимися брутто-коэффициентамн. &12 ], а над растворами хлоридов - [ bt2 ] и [ Bid ], так как комплексные ионы нелетучи. Только для растворов солей, не образующих комплексов с бромом ( сульфаты, нитраты) приводимые в литературе [ I, б ] значения Нэ являются истинными коэффициентами распределения брома. [13]
Страницы: 1