Практический осмотический коэффициент
Cтраница 1
Практический осмотический коэффициент приложим к очень разведенным растворам, когда величина N2 мала. [1]
Практический осмотический коэффициент может служить одной из самых надежных характеристик растворов полиэлектролитов, тем более что результаты определения ФР различными методами [10--12] хорошо согласуются друг с другом. Главным фактором, определяющим величину фр, является плотность электрических зарядов вдоль цепи полимера, причем при увеличении плотности зарядов Фр резко падает. [2]
Практический осмотический коэффициент может служить одной из самых надежных характеристик растворов полиэлектролитов, тем более что результаты определения Фр различными методами [10-12] хорошо согласуются друг с другом. Главным фактором, определяющим величину фр, является плотность электрических зарядов вдоль цепи полимера, причем при увеличении плотности зарядов ФР резко падает. [3]
Практический осмотический коэффициент срр не только не увеличивается с разбавлением, а даже иногда уменьшается, что. [4]
Практический осмотический коэффициент рр не только не увеличивается с разбавлением, а даже иногда уменьшается, что противоречит характеру изменения свойств и ионных ассоциатов ( модель Раиса - Гарриса), и обычных низкомолекулярных сильных электролитов. Разбавление растворов полиэлектролитов сопровождается связыванием противоионов, что подтверждает большую роль электростатического поля, образованного цилиндрическим симметричным полимерным стержнем. [5]
ФР - практический осмотический коэффициент, который включает все отклонения от идеальности, связанные только с противоионами. [6]
Фр - практический осмотический коэффициент, который включает все отклонения от идеальности, связанные только с противоионами. [7]
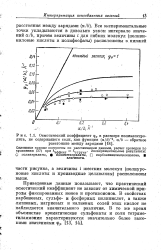 |
Осмотический коэффициент фр в растворе полиэлектролита, не содержащего соли, как функция ( а / Ь 1, а / Ь - обратное. [8] |
Приведенные данные показывают, что практический осмотический коэффициент не зависит от химической природы фиксированных ионов и противоионов. В свойствах карбоновых, сульфо - и фосфорных поликислот, а также литиевых, натриевых и калиевых солей этих кислот не наблюдается значительного различия. [9]
Экспериментальные данные по осмотическому давлению некоторых растворов приведены в Приложении I, а значения практических осмотических коэффициентов - в Приложении II. Методы экспериментального определения значений этих параметров рассмотрены на стр. Для растворов, опытные значения я и Ф которых отсутствуют или вызывают сомнение, могут быть использованы методы расчета осмотических давлений, приведенные ниже. [10]
Однако реально измеренное осмотическое давление в растворе полиэлектролита я всегда отличается от яид; обычно я меньше, чем яид. Поэтому используют уравнение Вант-Гоффа, введя в него практический осмотический коэффициент Ф, учитывающий все отклонения от идеальности, связанные с противо-ионами. Величина Ф я / яид служит одной из самых основных характеристик полиэлектролитов. [11]
Однако реально измеренное осмотическое давление в растворе полиэлектролита я всегда отличается от яид; обычно я меньше, чем яид. Поэтому используют уравнение Вант-Гоф - фа, введя в него практический осмотический коэффициент Ф, учитывающий все отклонения от идеальности, связанные с про-тивоионами. Величина Фя / лид служит одной из самых основных характеристик полиэлектролитов. [12]
Страницы: 1