Дробный коэффициент
Cтраница 1
 |
В частном случае при. [1] |
Дробные коэффициенты берутся с целью получения более простых выражений для напряжений. [2]
Дробные коэффициенты вводят в уравнение потому, что теплоту реакции относят к одному молю образовавшегося соединения. Данное термохимическое уравнение показывает, что при образовании одного моля окиси азота в - реакцию вступает половина моля свободного азота ( 14 г) и половина моля кислорода ( 16 г); при этом процессе поглощается указанное количество теплоты. [3]
Использование дробных коэффициентов в конечном соотношении сил и моментов, предложенном И. И. Казакевичем, значительно усложняет решения. [4]
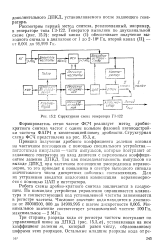 |
Структурная схема генератора ГЗ-122. [5] |
Принцип получения дробного коэффициента деления основан на частичном поглощении с помощью специального устройства - поглотителя импульсов - части импульсов, которые поступают от задающего генератора на вход делителя с переменным коэффициентом деления ДПКД. Так как последовательность импульсов на выходе ДПКД при частичном поглощении распределена неравномерно, то это приведет к появлению в спектре выходного сигнала значительного числа дискретных побочных составляющих. Для их устранения вводится аналоговая компенсация неравномерности с помощью ЦАП и интегратора. [6]
Интерполяционные многочлены с дробными коэффициентами следует сразу отбросить. [7]
Она принимается за знаменатель дробных коэффициентов, по которым вычисляются величины ежегодных норм. [8]
Иногда встречаются записи уравнений с дробными коэффициентами. Означает ли такой коэффициент перед формулой вещества, что в реакцию вступает какая-то часть молекулы вещества. [9]
Поэтому в термохимических уравнениях вполне допустимы дробные коэффициенты. Кроме того, обычно тепловые эффекты реакций указывают нри стандартной температуре 25 С. [10]
Если числитель и знаменатель алгебраической дроби являются многочленами с дробными коэффициентами, то для ее упрощения целесообразно умножить числитель и знаменатель на общий знаменатель всех коэффициентов. [11]
В практике ( см. ГОСТ 2.317 - 69) не применяют дробные коэффициенты искажения и заменяют их целыми числами - единицами. [12]
Приведенный пример является первым случаем применения правила Пирсона для соединений с дробными коэффициентами в химических формулах, как видим, правило и для этих случаев хорошо выполняется. [13]
Поскольку в термохимических уравнениях формулы означают моли или грамм-атомы, то здесь допускаются и дробные коэффициенты. [14]
Теплота образования всегда дается на одну грамм-молекулу вещества, поэтому в термохимических уравнениях допустимы дробные коэффициенты; формулы в этом случае обозначают не молекулы, а грамм-молекулы реагирующих веществ. Приведенное термохимическое уравнение показывает, что при образовании 1 моль ( 18 г) воды из 1 моль водорода ( 2 г) и 1 / 2 моль кислорода ( 16 г) выделяется 68 4 ккал ( 286 6 кдж) теплоты. [15]
Страницы: 1 2 3 4