Стехиометрический коэффициент - вещество
Cтраница 1
Стехиометрический коэффициент вещества не является его константой, а зависит от типа реакции. Многие вещества, применяемые для приготовления титрантов, в зависимости от условий реакции изменяют свои химические свойства и могут поэтому иметь различные стехиометрические коэффициенты. [1]
Стехиометрические коэффициенты веществ в уравнениях ( 187), ( 189) и ( 191) должны браться с соответствующими принятому правилу знаками. [2]
Обычно считают стехиометрические коэффициенты веществ, вступающих в реакцию, отрицательными, а получающихся при реакции, положительными. [3]
Под соответствующей степенью понимают стехиометрический коэффициент вещества в рассматриваемой реакции. [4]
Для этого составляют стехиометрическую матрицу ( Г) - матрицу, элементами которой являются стехиометрические коэффициенты веществ, участвующих в реакциях и определяют ранг матрицы. Ранг стехиометрической матрицы ( Г) отвечает числу независимых реакций - базису реакций и числу ключевых веществ. [5]
Я) кон и Hi 2 ( пЯ) нач - суммарные энтальпии прь-дуктов и исходных веществ, п - стехиометрические коэффициенты веществ в уравнении реакции. [6]
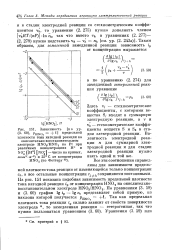 |
Зависимость [ по ур. ( 3. 60, PHNOS 1 ] предельной плотности тока катодной реакции на. [7] |
Здесь Vj - стехиометрические коэффициенты, с которыми вещества Sj входят в суммарную электродную реакцию, a v и v - стехиометрические коэффициенты веществ S и 8& в стадии электродной реакции. [8]
Как уже сказано, подавляющее большинство химических реакций протекает ио стадиям, поэтому порядок реакции не может быть определен как сумма стехиометрических коэффициентов веществ, вступающих в химическую реакцию. Для определения порядка реакции необходимо сначала установить порядок реакции по каждому веществу, вступающему в реакцию. Сумма порядков реакции по каждому веществу и дает общий порядок реакции в целом. Для того чтобы можно было определить порядок по данному веществу, необходимо создать такие условия, при которых будет изменяться концентрация только этого вещества. [9]
Как уже сказано, подавляющее большинство химических реакций протекает по стадиям, поэтому порядок реакции не может быть определен как сумма стехиометрических коэффициентов веществ, вступающих в химическую реакцию. Для определения порядка реакции необходимо сначала установить порядок реакции по каждому веществу, вступающему в реакцию. Сумма порядков реакции по каждому веществу и дает общий порядок реакции в целом. Для того чтобы можно было определить порядок по данному веществу, необходимо создать такие условия, при которых будет изменяться концентрация только этого вещества. [10]
S ( п Я) кон и HI 2 ( пЯ) нач - суммарные энтальпии прб-дуктов и исходных веществ, п стехиометрические коэффициенты веществ в уравнении реакции. [11]
Обобщим несколько понятие стехиометрического коэффициента, введенное в главе I. Будем записывать стехиометрические коэффициенты веществ, принимающих участие в прямой элементарной реакции, со знаком минус, а стехиометрические коэффициенты веществ, участвующих в обратной реакции, - со знаком плюс. [12]
Обобщим несколько понятие стехиометрического коэффициента, введенное в главе I. Будем записывать стехиометрические коэффициенты веществ, принимающих участие в прямой элементарной реакции, со знаком минус, а стехиометрические коэффициенты веществ, участвующих в обратной реакции, - со знаком плюс. [13]
Эта связь выражается уравнениями, подобными зависимости ( Х-1), которые называют кинетическими. Из уравнения ( Х-1) видно, что скорость реакции зависит также от величины стехиометрических коэффициентов веществ, участвующих в превращении. Эти величины входят в качестве показателей степени при концентрациях, а их сумма называется порядком реакции. [14]
Тепловые эффекты реакций, приводимые в справочных таблицах, - обычно относятся к 1 кмолю одного из веществ, участвующих в реакции. Это значение теплового эффекта ( изменение функции состояния) одновременно относится ( см. гл. VIII, § 1) к определенным количествам других веществ, равным соответственно величинам стехио-метрических коэффициентов этих веществ в уравнении реакции, при условии, что стехиометрический коэффициент вещества, на 1 кмоль которого дается тепловой эффект, равен единице. [15]
Страницы: 1 2