Атом - кобальт
Cтраница 1
Атом кобальта находится в центре ядра, образуемого четырьмя пятичленными кольцами ( рис, 10.7), и связан, с одной стороны, с бензимидазольной группой, а с другой - с цианидной группой. [1]
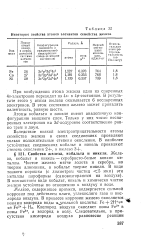 |
Некоторые свойства атомов элементов семейства железа. [2] |
Атомы кобальта и никеля имеют аналогичную конфигурацию внешнего слоя. Только у них число неспаренных электронов на Зй-подуровне соответственно равно трем и двум. [3]
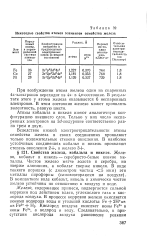 |
Некоторые свойства атомов элементов семейства железа. [4] |
Атомы кобальта и никеля имеют аналогичную конфигурацию внешнего слоя. Только у них число неспаренных электронов на Sd-подуровне соответственно равно трем и двум. [5]
Атомы кобальта и никеля имеют аналогичную конфигурацию внешнего слоя, только у них число неспаренных электронов на З - подуровне соответственно равно трем и двум. [6]
Атом кобальта взаимодействует с кратной связью N O и находится от нее на расстоянии 1 1 А. Расстояние Со-N составляет 1 7 А. [7]
Атомы кобальта и атомы углерода, связанные с ними формально простыми связями, расположены в одной плоскости. [8]
Атом кобальта координирован тремя атомами азота тридентатного органического лиганда и двумя атомами хлора. [9]
Атом кобальта имеет заполненную электронную оболочку, свойственную редким газам ( криптону), и как протон, так и анион могут быть легко сольватированы. Однако ограниченная растворимость гидрокарбонила в воде и гораздо более легкая растворимость его в органических растворителях несколько загадочны. Данные, согласующиеся с кислотным типом катализа, будут кратко рассмотрены. [10]
Атом кобальта обладает семью Sd-электронами, а никеля - восемью. В следующем за никелем атоме меди оказывается сразу 10 Sd-электронов. Одному 4з - электрону оказывается выгодно перейти в 3d - cocTOHHHe, чтобы полностью заполнить третью оболочку. [11]
Атом кобальта имеет 27 электронов. Присоединение пятого лиганда невозможно, так как в таком случае будет превзойдено число электронов атома криптона. Недостающий электрон поэтому предоставляет другой атом кобальта, который тоже присоединяет 4 молекулы окиси углерода. Другими словами, между двумя атомами кобальта должна образоваться ковалентная связь. Исследование этого соединения показывает, что оно действительно является димером. [12]
Атомы кобальта, входящие в состав бисдегидрокоррина ( БДГК) и корриноидных комплексов, имеют сходное электронное строение. Следовательно, сопряжение двойных связей, находящихся на периферии колец А и D в БДГК, с внутренним двойными связями отсутствует. Эти эффекты обусловлены взаимодействием 1 3-диаксиального типа между ангулярнымк метальными группами БДГК, находящимися в положениях С-1 и С-19, и приближающимся алкильным лигандом. Фотолиз метилированных и этилированных комплексов Со ( III) ( БДГК) в анаэробных условиях приводит к обычному гемолитическому расщеплению связи Со-С. [13]
Атом кобальта имеет заполненную электронную оболочку, что согласуется с диамагнетизмом комплекса. [14]
Атом кобальта обладает семью Sd-электронами, а никеля - восемью. Одному 45-электрону оказывается выгодно перейти в Sd-состояние, чтобы полностью заполнить третью оболочку. [15]
Страницы: 1 2 3 4