Атом - металл
Cтраница 2
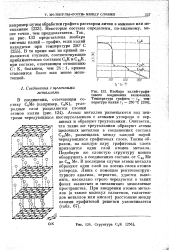
Атомы металлов размещаются над центрами чередующихся шестиугольников с атомами углерода в вершинах и образуют треугольники. Считается, что такие же треугольники образуют атомы щелочных металлов в соединениях состава С16Ме, размещаясь между каждой парой чередующихся графитовых слоев. Таким образом, на каждую пару графитовых слоев приходится один слой атомов металла. [17]
Атомы металлов, теряя электроны, превращаются в элементарные положительные ионы. [18]
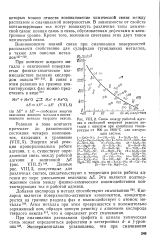 |
Связь между работой адгезии и свободной энергией реакции металла с окислом при колебании температуры от 900 до 1900 С для следующих систем. [19] |
Атом металла при этом превращается в положительно заряженный ион, образуя ионную решетку с анионами кислорода твердого окисла 519, что и определяет рост смачивания. [20]
Атомы металлов и водорода удерживают валентные электроны слабее серы. Таким образом, сера в соединениях с водородом или металлами отрицательно валентна. То же имеет место и в отношении других металлоидов. [21]
Атомы металлов, отдавая электроны другим элементам, окисляются, играя при этом роль восстановителей. [22]
Атом металла на поверхности нормальной кристаллографической плоскости будет образовывать л-связь со значительно большим числом атомов металла, чем атом металла, расположенный на ребре или угле. В первом случае адсорбированная молекула окиси углерода должна конкурировать с большим числом атомов металла за d - электроны, чтобы образовать л-связь. [23]
Атомы металла окружены подобными им атомами. Каждый из них имеет на внешней электронной оболочке лишь несколько электронов, которыми они владеют сообща. Такая атомная связь характерна для всех металлов. Именно поэтому металлы служат проводниками электрического тока, могут, быть сплавлены или сварены друг с другом. Обобществленные электроны образуют своеобразный электронный газ, плотность которого, например, в меди может составить 1023 электронов в кубическом сантиметре. [24]
Атомы металлов могут образовывать химические связи обычным способом, обобществляя электронные пары, как в молекуле газообразного хлорида титана TiCLj. Это соединение используют для получения чистого металлического титана, применяемого в авиастроении. Например, в пентакарбониле железа Fe ( CO) s каждая молекула моноксида углерода отдает пару электронов на вакантную валентную орбиталь атома железа. В результате образуется устойчивая молекула со структурой бипирамиды. Молекулы моноксида углерода или другие молекулы, которые могут занимать их место в таких соединениях, называют лигандами. В молекуле Fe ( CO) s часть лигандов или все лиганды могут замещаться на другие доноры электронов ( основание Льюиса), такие как моноксид азота NO, аммиак МНз, ионы галогенов F -, С1 -, Вг -, вода НаО, цианид-ион CN - и многие другие. В результате образуется большой ряд соединений. По отношению к некоторым атомам металла в качестве лиганда может выступать даже молекула азота NZ. В таком случае она становится более реакционноспособной, т.е. активируется. Это один из приемов, который химики-металлоорганики стремятся использовать, чтобы создать новые катализаторы для фиксации азота, т.е. для превращения N2 в аммиак МНз, который служит исходным продуктом в производстве удобрений. [25]
Атомы металлов, например, в литийалкилах или реактивах Гриньяра ( эти соединения содержат в основном ковалентные связи) также являются донорами электронов; это приводит к отрицательно поляризованному атому углерода в каждом случае: R - - Lj и R - - MgHaI ( ср. [26]
 |
Структура х-карбидов, в которой октаэдры [ МевХ ] сочленяются вершинами. Атомы непереходного металла, такого, как А1, могут быть расположены в. [27] |
Атомы металла в позициях 6 ( ft) II и 12 ( fe) образуют каркас слегка деформированных октаэдров, в котором все атомы в вершинах принадлежат одновременно двум октаэдрам. [28]
 |
Удельные веса металлов весом 053. таким образом, са. [29] |
Атомы металлов могут только отдавать, но не принимать электроны - проявлять только электроположительную валентность. Но наиболее общее химическое свойство металлических элементов, отличающее их от неметаллических, заключается з способности металлов образовывать свободные ( хотя и гидратировэнные) положительные ионы. [30]
Страницы: 1 2 3 4