Атом - щелочноземельный металл
Cтраница 3
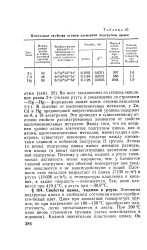 |
Некоторые свойства атомов элементов подгруппы цинка. [31] |
В отличие от щелочноземельных металлов, у Zn, Cd и Hg предвнешний энергетический уровень содержит не 8, а 18 электронов. Это приводит к существенному отличию свойств рассматриваемых элементов от свойств щелочноземельных металлов. Ввиду того, что на внешнем уровне атомы элементов подгруппы цинка, как и атомы щелочноземельных металлов, имеют по два s - эле-ктрона, существует некоторое сходство между элементами главной и побочной подгруппы II группы. Атомы ( и ионы) подгруппы цинка имеют меньшие размеры, чем атомы ( и ионы) соответствующих элементов главной подгруппы. Поэтому у цинка, кадмия и ртути химическая активность менее выражена, чем у элементов главной подгруппы: при обычной температуре они труднее окисляются и не взаимодействуют с водой. Плотность этих металлов возрастает от цинка ( 7130 кг / м3) к ртути ( 13600 кг / м3), а температуры плавления и кипения, а также твердость - понижаются. Так, цинк плавится при 419 4 С, а ртуть при - 38 9 С. [32]
К данной подгруппе относятся цинк, кадмий и ртуть. Это приводит к существенному отличию свойств рассматриваемых элементов от свойств щелочноземельных металлов. Ввиду того, что на внешнем уровне атомы элементов подгруппы цинка, как и атомы щелочноземельных металлов, имеют по два s - эле-ктрона, существует некоторое сходство между элементами главной и побочной подгруппы II группы. Атомы ( и ионы) подгруппы цинка имеют меньшие размеры, чем атомы ( и ионы) соответствующих элементов главной подгруппы. Поэтому у цинка, кадмия и ртути химическая активность менее выражена, чем у элементов главной подгруппы: при обычной температуре они труднее окисляются и не взаимодействуют с водой. [33]
Все атомы рассматриваемой подгруппы являются восстановителями. Но восстановительная способность их резко падает от цинка к ртути. Объяснение этому следует искать в том, что их соседний с наружным электронный слой состоит из 18 электронов с заполненным d - подуровнем, радиусы нейтральных атомов этих элементов значительно меньше радиусов атомов щелочноземельных металлов - кальция, стронция и бария, входящих во 2А подгруппу s - элементов. [34]
Только немногие из радиоактивных элементов, например, торий, мезаторий, уран, радий, могут быть получены в весовых количествах. Исследование свойств этих эле-менгов происходит по обычным химическим методам; радиоактивность не оказывает влияния на химические свойства атомов; атом радия, например, пока он не распался, обладает всеми характерными свойствами атомов щелочноземельных металлов. [35]
К данной подгруппе относятся цинк, кадмий и ртуть. В отличие от щелочноземельных металлов, у Zn, Cd и Hg предвнешний энергетический уровень содержит не 8, а 18 электронов. Это приводит к существенному отличию свойств рассматриваемых элементов от свойств щелочноземельных металлов. Ввиду того, что на внешнем уровне атомы элементов подгруппы цинка, как и атомы щелочноземельных металлов, имеют по два s - эле-ктрона, существует некоторое сходство между элементами главной и побочной подгруппы II группы. Атомы ( и ионы) подгруппы цинка имеют меньшие размеры, чем атомы ( и ионы) соответствующих элементов главной подгруппы. Поэтому у цинка, кадмия и ртути химическая активность менее выражена, чем у элементов главной подгруппы: при обычной температуре они труднее окисляются и не взаимодействуют с водой. [36]
Страницы: 1 2 3