Атом - никель
Cтраница 1
Атомы никеля, связанные с поверхностным слоем одной связью, благодаря большой ненасыщенности адсорбируют молекулы адсорбтива сильнее или в большем количестве, чем атомы никеля, связанные с поверхностью двумя связями. В свою очередь, на последних адсорбция проходит интенсивнее, чем на атомах никеля, связанных с поверхностью большим числом связей. [1]
Атомы никеля, расположенные на поверхности, связаны с другими атомами, находящимися внутри кристалла, но их валентности, направленные из глубины кристалла наружу, насыщены неполностью. Можно ожидать, что атомы, расположенные на поверхности, окажутся в состоянии вступать в контакт с различного типа соединениями, образуя поверхностный слой, в котором их валентности будут насыщены. Экспериментально было показано, что этилен взаимодействует с поверхностью никеля экзотермично ( приблизительно - 60 ккал. [2]
Атомы никеля, расположенные на поверхности, связаны с другими атомами, находящимися внутри кристалла, но их валентности, направленные из глубины кристалла наружу, насыщены не полностью. Можно ожидать, что атомы, расположенные на поверхности, окажутся в состоянии вступать в контакт с различного типа соединениями, образуя поверхностный слой, в котором их валентности будут насыщены. Экспериментально было показано, что этилен взаимодействует с поверхностью никеля экзотермично ( приблизительно - 60 ккал / моль) и обратимо. Хотя структура комплекса этилен - никель неизвестна, в образовании связи с никелем должны участвовать электроны двойной связи, поскольку насыщенный углеводород, например этан, не проявляет тенденции к взаимодействию с поверхностью никеля. На рис. 7 - 3 приведена возможная структура такого комплекса, в котором пунктирные линии означают частичные ( парциальные) связи; образование полной связи углерод - никель не предполагается, а реакционноспособная половина двойной связи является ослабленной, но, по-видимому, полностью не разорванной. [3]
Атомы никеля, расположенные на поверхности, связаны с другими атомами, находящимися внутри кристалла, но их валентности, направленные из глубины кристалла наружу, насыщены неполностью. Можно ожидать, что атомы, расположенные на поверхности, окажутся в состоянии вступать в контакт с различного типа соединениями, образуя поверхностный слой, в котором их валентности будут насыщены. Экспериментально было показано, что этилен взаимодействует с поверхностью никеля экзотермично ( приблизительно - 60 ккал / молъ) и обратимо. [4]
Атомы никеля при этом образуют ровный стой металла на поверхности предмета. [5]
 |
Межатомные расстояния и валентные углы в молекуле этилксан. [6] |
Атом никеля занимает частное положение в начале координат. [7]
Атом никеля, несущий два положительных заряда и образующий четыре ковалентные й р2 - связи, имеет лишь четыре Sd-орбитали, доступные для восьми неподеленных Зй-электронов, которые, таким образом, должны образовать четыре пары, причем квадратный комплекс NiX4 будет диамагнитным. Двухзарядный положительный ион никеля в комплексе, образованном только с участием 4s - и 4р - орбиталей ( электростатические связи или слабые ковалентные связи), распределяет восемь Зй-электронов между пятью Зй-орбиталями таким образом, чтобы оставалось два неспаренных электрона; при этом комплекс имеет магнитный момент, равный 2 83 магнетона Бора. Отсюда следует, что по данным магнитных измерений можно установить принадлежность комплексов никеля к тетраэдрическому или к плоскоквадратному классу. [8]
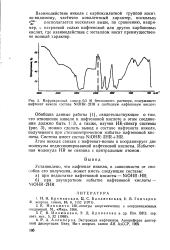 |
Инфракрасный спектр 0 5 М бензольного раствора, содержащего нафтенат никеля состава NiOHR 2HR и свободную нафтеновую кислоту. [9] |
Атом никеля связан с нафтенат-ионом и координирует две молекулы недиссоциированной нафтеновой кислоты. Избыточная молекула HR не связана с центральным атомом. [10]
Атомы никеля, расположенные по углам правильного равностороннего треугольника ( рис. Збв), не взаимодействуют между собой: каждый из них координирован СО-группой, атомом азота пгаперидинового ли-ганда на равных расстояниях 1 75 А и формально тройной связью C N длиной 1 13 А соседнего фрагмента на расстоянии 1 99 А от центра связи. Авторами [189] отмечен тот факт, что атомы Ni ( i) и Ni 2) находятся на довольно близких расстояниях 3 20 А от двух атомов Ni соседних тримерных молекул. Это обстоятельство, как и то, что лиганды не сообщают атомам Ni устойчивой 18-электронной конфигурации, заставляет предположить существование системы металл-донорных связей. [11]
Атомы никеля в кристаллической решетке не заряжены и являются мягкими кислотными центрами, к которым присоединяются мягкие основные молекулы СО, имеющие свободную пару электронов. Четыре сг-связи между центральными атомом никеля и атомами углерода молекул СО усиливаются я-датив-ными связями, причем электроны заселенных d - орбиталей никеля принимают участие в образовании этой связи за счет незаселенных я-орбиталей атома углерода. Тем самым высокая электронная плотность нейтрального атома металла, которая особенно велика для атомов с низкой степенью окисления, перераспределяется на лиганды, в результате чего достигается более равномерное распределение электронной плотности по всей молекуле. [12]
Атомы никеля, связанные с поверхностным слоем одной связью, благодаря большой ненасыщенности адсорбируют молекулы адсорбтива сильнее или в большем количестве, чем атомы никеля, связанные с поверхностью двумя связями. В свою очередь, на последних адсорбция проходит интенсивнее, чем на атомах никеля, связанных с поверхностью большим числом связей. [13]
Атомы никеля при этом образуют ровный слой металла на поверхности предмета. [14]
Атом никеля имеет 28 электронов. Присоединение каждой молекулы СО увеличивает эффективный номер никеля на два. [15]
Страницы: 1 2 3 4