Атом - бензол
Cтраница 1
Атомы бензола в этих условиях не обмениваются. Электроноакцеп-торные заместители резко уменьшают скорость водородного обмена. В ацетилферроцене водороды пятичленных колец обмениваются в 1000 раз медленнее, чем в ферроцене kl 5 - 10 - 7 сек-1. Скорость водородного обмена фенил - я М - дифенилферроцена несколько меньше скорости обмена для ферроцена. Электронодонорные заместители повышают скорость обмена. [1]
На рис. 22 указаны свободные валентности атомов бензола и нафталина, полученные вторым способом. [2]
Из этана и этилена известны свойства простых и двойных связей; мы приписываем их атомам бензола и обнаруживаем, что полученная картина не соответствует реальности. [3]
В схеме, изображенной ниже, стрелками отмечены те атомы углерода пиридинового кольца, которые по своим свойствам сравнимы с атомами бензола, а звездочкой - положения, испытывающие значительное влияние кольцевого атома азота. Аналогичные свойства соответствующих положений кольцевой системы характерны и для других гетероциклов такого типа. [4]
Однако поведение бензола в химических реакциях показывает, что он очень сильно отличается от обычных ненасыщенных соединений и что связи между всеми шестью атомами бензола одинаковы и не похожи на связи между атомами углерода ни в предельных алифатических углеводородах, ни в углеводородах ненасыщенных. Чтобы отобразить в структурных формулах особенности распределения электронных облаков л-электронов по связям, для обозначения смещенных я-электронов формулы иногда дополняют изогнутыми стрелками, как это показано при изображении формул бутадиена и бензола. [5]
Ароматические диазосоединения открыл Петер Грисс ( 1858); он избрал для впервые полученных им веществ название диа-зо, предполагая, что два водородных атома бензола замещены двумя атомами азота. Первоначальный метод диазотирования аминов Грисса заключался в применении окислов азота в спиртовом растворе. Метод Грисса был затем заменен методом Кне-венагеля, где для диазотирования предложены эфиры азотистой кислоты. [6]
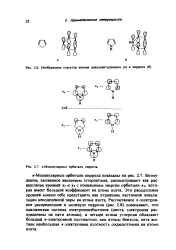 |
Изображение структур аниона циклопеитадиеинла ( а и пиррола ( 6. [7] |
Рассчитанное т-электрон-ное распределение в молекуле пиррола ( рис. 2.8) показывает, что циклическая система электроноизбыточна ( шесть электронов распределены на пяти атомах), и четыре атома углерода обладают большей т-электронной плотностью, чем атомы бензола, хотя все-таки наибольшая т-электронная плотность сосредоточена на атоме азота. [8]
Изучение кинетики изотопного обмена водорода в ферроцене и его производных позволяет количественно оценить изменение реакционной способности под влиянием заместителей при элек-трофильном замещении, а также провести количественное сравнение с бензолом и соответствующими его производными и другими ароматическими системами. Атомы бензола в этих условиях не обмениваются. Электроноакцеп-торные заместители резко уменьшают скорость водородного обмена. [9]
В общем, чтобы описать положения всех атомов бензола СеН6, необходимо 3X12 36 координат. Однако в каждой молекуле бензола имеется большой набор элементов симметрии: одна ось 6-го порядка, шесть осей 2-го порядка, семь плоскостей симметрии и центр симметрии. Порядок этой группы равен 24 ( 6X2x2), а атомов углерода всего шесть, поэтому каждый из них должен быть расположен на оси или в плоскости симметрии, так что симметрия непосредственного окружения каждого атома имеет порядок 4 24 / 6; то же самое относится к атомам водорода. В рассматриваемом примере оба типа атомов должны располагаться на осях 2-го порядка, через которые проходят две плоскости симметрии. [10]
В общем, чтобы описать положения всех атомов бензола Cell, необходимо 3X12 36 координат. Однако в каждой молекуле бензола имеется большой набор элементов симметрии: одна ось 6-го порядка, шесть осей 2-го порядка, семь плоскостей симметрии и центр симметрии. Порядок этой группы равен 24 ( 6) 2х2), а атомов углерода всего шесть, поэтому каждый из них должен быть расположен на оси или в плоскости симметрии, так что симметрия непосредственного окружения каждого атома имеет порядок 4 24 / 6; то же самое относится к атомам водорода. В рассматриваемом примере оба типа атомов должны располагаться на осях 2-го порядка, через которые проходят две плоскости симметрии. [11]
Страницы: 1