Атом - рубидий
Cтраница 3
Начиная с рубидия, заполняется Ss-подуровень; это тоже соответствует второму правилу Клечковского. У атома рубидия ( Z 37) появляется характерная для щелочных металлов структура с одним s - электроном во внешнем электронном слое. Тем самым начинается построение нового - пятого - периода системы элементов. При этом, как и при построении четвертого периода, остается незаполненным rf - подуровень предвнешнего электронного слоя. Напомним, что в четвертом электронном слое имеется уже и / - подуровень, заполнения которого в пятом периоде тоже не происходит. [31]
Начиная с рубидия, заполняется Бз-подуровспь; это тоже соответствует второму правилу Клечковского. У атома рубидия ( Z 37) появляется характерная для щелочных металлов структура с одним s - электроиом во внешнем электронном слое. Тем самым начинается построение нового - пятого - периода системы элементов. [32]
Заполнение электронами энергетических уровней в атомах элементов пятого периода происходит в той же последовательности, как и в атомах четвертого периода. В атоме рубидия ( № 37) начинает формироваться пятый энергетический уровень: на s - подуровне находится один электрон. В атоме стронция ( № 38) на Ss-подуровне имеются два электрона с противоположными спинами. Начиная с иттрия ( № 39), заполняется d - подуро-вень четвертого энергетического уровня, после этого заполняется 5р - подуровень. [33]
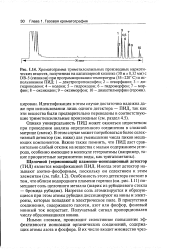
Определить значение проекции магнитного момента электрона цн на направление магнитного поля, если известно, что величина расщепления пучка на экране А / 2 мм и скорость атомов v - 500м / сек. Узкий пучок атомов рубидия ( в нормальном состоянии) пропускается через поперечное сильно неоднородное магнитное поле протяженностью / 4 10 см ( рис. 7.2.) При каком значении градиента напряженности магнитного поля величина расщепления пучка на экране, отстоящем на расстоянии 12 15 см от магнита, равна А / 3 мм. [34]
На рис. 13.1 приведена общая схема прекрасного эксперимента, выполненного в институте квантовой оптики имени Макса Планка ( Гархинг, Германия), в котором реализована идея микромазера. Сильно коллимированный пучок атомов рубидия пропускается через селектор скоростей Физо. Перед входом в резонатор атомы возбуждаются на верхний мазерный уровень бЗрз / 2 - Сверхпроводящий ниобиевый резонатор охлаждается до температуры 0 5 К с помощью гелиевого ( 3Не) криостата. [35]
Щелочной ( термоионный) пламенно-ионизационный детектор ( ТИД) является модификацией ПИД. Нагретая соль атомизируется и образующиеся при этом атомы рубидия диссоциируют на ионы и электроны, которые попадают в электрическое поле. В присутствии соединения, содержащего галоген, азот или фосфор, фоновый ионный ток возрастает. Получаемый сигнал пропорционален числу образовавшихся ионов. [37]
Изучен частный случай очень низких температур, когда почти все электроны проводимости спарены в бозоны Купера. Обоснована возможность перехода кристалла CsjCeo в сверхпроводящее состояние при появлении атомов рубидия и образовании кристалла CsiRbCai. Установлен критерий для энергетических констант кристалла, при которых возможен фазовый переход в сверхпроводящее состояние. [38]
Возможно, что в ближайшем будущем рубидий станет основным материалом для фотокатодов и оттеснит цезий на второе место. Применение рубидия для изготовления различных фотокатодов основано на легкой ионизации атомов рубидия под действием волн света. [39]
В атомных эталонах ( стандартах) частоты используются квантовые переходы между энергетическими уровнями атомов вещества. В настоящее время для создания стандартов частоты кроме атомов цезия используются также атомы рубидия и водорода. Поэтому эталоны частоты или генераторы колебаний называют цезиевыми, рубидиевыми или водородными. Атомный стандарт частоты, снабженный синхронными часами, называют атомными часами. [40]
Высокая химическая активность щелочных металлов объясняется тем, что наружные электроны у них сравнительно слабо связаны с ядром. С увеличением зарядов ядер атомов вследствие увеличения радиусов атомов связь валентных электронов ослабевает, поэтому атомы рубидия особенно легко отдают электроны. Однако на химическую активность оказывают большое влияние и размеры образующихся ионов. Размеры ионов уменьшаются от цезия к литию. Поэтому литий вступает в более прочную связь с большинством неметаллов, например с кислородом. Литий сгорает с выделением наибольшего количества теплоты. [41]
Металлические Rb и Cs по химическим свойствам очень похожи на калий, но проявляют большую химическую активность. На высокой химической активности основано их использование в качестве геттеров ( газопоглотителей) в вакуумных электронных приборах. Атомы рубидия и цезия настолько непрочно удерживают валентные электроны, что их могут выбить кванты света. На этом основано использование этих металлов для получения фототока в фотоэлементах. [42]
Возможность применения этого принципа к решению рассматриваемой проблемы была впервые высказана Бийвоетом ( Bijvoet, 1949 и 1955) и осуществлена на практике Пеердеманом, ван Боммелем и Бийвоетом ( Peerdeman, van Bommel, Bijvoet, 1951) на структуре смешанного ( - Ь) - тартрата натрия и рубидия. Кристаллическая структура этого соединения в то время уже была известна. Используя излучение циркониевого анода, возбуждающее атом рубидия, можно было рассчитать интенсивности для 15 пар отражений hkl и Jik l, предположив, что тартрат-ион обладает конфигурацией, показанной на схеме IX и согласующейся с обозначениями Фишера. [43]
В настоящее время изготавливаемые соли рубидия применяются главным образом для производства различных фотокатодов. Возможно, что в ближайшем будущем рубидий станет основным материалом для фотокатодов и оттеснит цезий на второе место. Применение рубидия для изготовления различных фотокатодов основано на легкой ионизации атомов рубидия под действием волн света. [44]
Однако расстояния между аналогичными атомами у этих веществ несколько различны. Так, например, кратчайшее расстояние между атомами натрия и хлора а / 2 ( в структуре NaCl) равно 2 81 А, между атомами калия и хлора - 3 14 А, между атомами рубидия и хлора - 3 27 А. [45]
Страницы: 1 2 3 4