Атом - свинец
Cтраница 1
Атомы свинца и серы связаны в кристалле двумя электронами: свинец отдает их сере. Ну а как в случае, когда соот ношение 1: 1 нарушается. Если рядом с атомом свинца нет атома серы, электроны окажутся свободными - они-то и будут служить носителями тока. А таких случаев совсем не так мало, как может показаться. Конечно, отношение 1.000 5: 1 кажется почти равным единице, но если вспомнить, как много атомов в кристалле, то эта незначительная разница уже не покажется вам такой пустячной. [1]
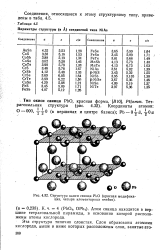 |
Структура окиси свинца РЬО ( красная модификация, четыре элементарных ячейки. [2] |
Атом свинца находится в вершине тетрагональной пирамиды, в основании которой расположены атомы кислорода. [3]
Атомы свинца и серы связаны в кристалле двумя электронами: свинец отдает их сере. Ну а когда соотношение 1: 1 нарушается. Если рядом с атомом свинца нет атома серы, электроны окажутся свободными - они-то и будут служить носителями тока. А таких случаев совсем не так мало, как может показаться. Конечно, соотношение 1 0005: 1 почти равно единице, но если вспомнить, как много атомов в кристалле, то эта незначительная разница уже не покажется вам такой пустячной. [4]
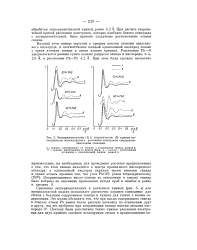 |
Экспериментальные ( 1 и теоретические ( 2 кривые интенсивности молекулярного рассеяния электронов свинцовоси-ликатными стеклами. [5] |
Каждый атом свинца окружен в среднем шестью атомами односвяз-ного кислорода, и соответственно каждый односвязный кислород связан с тремя атомами свинца и одним атомом кремния. [6]
 |
Процесс разряда свинцового аккумулятора. [7] |
Каждый атом свинца отрицательной пластины отдает два электрона. Вследствие - неболы шой растворимости сульфата свинца в электролите раствор быстро оказывается насыщенным. [8]
Сколько атомов свинца находится в I мл такого воздуха. [9]
Сколько атомов свинца находится в 1 мл такого воздуха. [10]
Наоборот, атомы свинца вытеснить и восстановить ионы из раствора цинковой соли не могут, и здесь практически никакой реакции не будет. [11]
Энергия ионизации атома свинца на 2164 - 1607 557 кДж / / моль больше, чем у атома стронция, что ведет к более сильному притяжению электронов. Орбитали атомов свинца имеют значительную плотность в направлении двух соседних атомов серы и это приводит к хорошему перекрыванию р-орбита-лей ионов серы и - свинца. Всего у атома серы имеются три р-электронные пары, а у атома свинца три свободные р-орби-тали. Тем самым осуществляется связывание в трех направлениях. Мезомерная ( резонансная) гомеополярная составляющая связи в сульфиде свинца больше, чем в сульфиде стронция. Вследствие двустороннего перекрывания р-орбиталей образуются резонансные цепи, в которых при удалении, например, одного электрона из иона S2 - возникает дефект, распределяющийся по всей цепи. Этим объясняется черный цвет и полупроводниковые свойства сульфида свинца. [12]
При избытке атомов свинца по сравнению со стехиометрическим составом образование дефектов происходит по Френкелю. При этом в качестве доноров выступают междоузельные ионы свинца. [13]
Поскольку избыток атомов свинца приводит к увеличению числа свободных электронов, а избыток халькогена дает свободные дырки, то существуют большие трудности в получении образцов с малыми концентрациями носителей заряда. [14]
 |
Антидетонационная эффективность смеси 60 % изооктана и 40 %. [15] |
Страницы: 1 2 3 4