Атом - цирконий
Cтраница 1
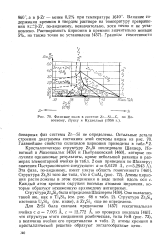 |
Фазовые поля в системе Zr-Si - С, по Новотному, Луксу и Кудиелька ( 1956 г.. [1] |
Атомы циркония расположены в этом соединении в виде цепей вдоль оси с. Каждый атом кремния окружен восемью атомами циркония, которые образуют искаженную архимедову антипризму. [2]
Размер атома циркония допускает существование координационного числа вплоть до 8, как, например, в его тетракисацетилацетонатном и оксалатном комплексах. По этой причине цирконий образует свои наиболее прочные комплексы с кислородсодержащими и другими анионными лигандами, в частности с фторид -, сульфат - и фосфат-ионами, которые дают скорее ионные, чем ковалентные связи. Получающиеся при этом ионы типа ZrFe2 - и [ Zr ( SO4) 4 ] 4 - растворимы в воде. [3]
Радиусы атомов циркония и гафния, а также радиусы их ионов ( Э4) из-за лантаноидного сжатия имеют почти одинаковые размеры. Поэтому свойства циркония и гафния очень близки. [4]
Таким образом, атомы циркония связаны фосфатными группами, причем половина атомов фосфора находится в плоскостях кристаллической решетки, а половина - в межплоскостных областях. Большинство материалов этого типа характеризуется отношением P / Zr, равным 1 7, и содержит также аморфную фракцию. Фосфат циркония представляет собой среднекислотный катионит, его применяют для разделения продуктов ядерного деления. Основной его недостаток - тенденция к гидролизу, особенно в щелочной среде. [5]
Вследствие больших размеров атомов циркония и гафния вокруг них может разместиться больше лигандов, чем вокруг атома титана. При к.ч. 8 связь осуществляется с помощью восьми гибридных орбиталей, максимальная электронная плотность которых направлена в сторону вершин додекаэдра или антипризмы. [6]
Для реакции доступны два атома циркония. [7]
Определим на основе концепции Полинга радиус атомов циркония в гексагональной решетке, считая заданным этот радиус в кубической. [8]
Такое предположение согласуется с некоторой двойственностью природы атома циркония, который, с одной стороны, принадлежит к элементам, не склонным образовывать ионных связей, с другой стороны, значительно отличается от элементов, образующих чисто ковалентные связи, например от углерода и кремния. [9]
Если катализатор действительно содержит четыре иона водорода на атом циркония, то надо полагать, что каталитической активностью обладает один или максимум два иона. [10]
Изобразите геометрическое строение такого катиона, зная, что атомы циркония ( IV) образуют квадрат и связаны попарно двумя мостнко-выми гидроксолигандами. [11]
Эта структура предполагает: цепочечное строение; связь между атомами циркония через оксомостики и фосфатные группы; наличие кислых фосфатных групп. Она достаточно хорошо объясняет свойства фосфатов, способность их к ионному обмену. При ионном обмене на катионы металлов замещается водород фосфатных групп; после их насыщения в обмене могут принимать участие и гидроксогруппы. В сильнощелочной среде фосфатные группы замещаются на гидроксогруппы, что приводит к изменению состава. Не исключено, что фосфаты имеют циклическое строение, а связь между атомами циркония осуществляется и через гидроксомостики. [12]
Предварительными опытами было установлено, что в осадке па каждый атом циркония приходится два атома фосфата, из чего следует, что состав осадка выражается формулой Zr ( HPO. [13]
Получивший наибольшее применение цир-конилфосфат является труднорастворимой солью, в которой на один атом циркония приходится два или меньше кислотных остатков ортофосфорной кислоты. [14]
Получивший наибольшее применение цир-конйлфосфат является труднорастворимой солью, в которой на один атом циркония приходится два или меньше кислотных остатков ортофосфорной кислоты. [15]
Страницы: 1 2 3 4