Атом - следующий элемент
Cтраница 1
Атомы следующих элементов - Mg, Al, Si, Р, S, C1 - имеют на третьем уровне соответственно два, три, четыре, пять, шесть, семь электронов. Каждый электрон любого уровня вращается по собственной орбите, лежащей в своей, отличной от других, плоскости. [1]
Атом следующего элемента периодической системы - лития - имеет уже три электрона. Литий представляет собой металл, по химическим свойствам очень похожий на натрий. Во всех своих соединениях он всегда одновалентен. Следовательно, из трех электронов атома лития один электрон связан с ядром атома значительно слабее и расположен дальше от ядра, чем два другие электрона. [2]
Атом следующего элемента периодической системы - лития - имеет уже три электрона. Литий представляет собой металл, по химическим свойствам очень похожий на натрий. Во всех своих соединениях он всегда одновалентен. Следовательно, из трех электронов атома лития один электрон связан с ядром атома значительно слабее и расположен дальше от ядра, чем два другие электрона. [3]
В атоме следующего элемента - гелия - добавляется еще один электрон в том же состоянии Is. Энергия связи каждого из ls - электронов в атоме гелия, однако, значительно больше, чем энергия связи электрона в атоме водорода. [4]
В атомах следующего элемента - кальция ( № 20) - 4я - под-уровень заполняют два электрона с различными спинами. [5]
Определить истинные массы атомов следующих элементов: а) хрома; б) марганца; в) вольфрама; г) ниобия. [6]
Каков заряд ядра атома следующих элементов: лития, углерода, кислорода, фтора, неона, натрия, алюминия, серы, хлора, кальция, железа, цинка, бария, ртути, урана. [7]
Изобразите электронные облака атомов следующих элементов: а) лития; б) бериллия; в) бора; г) углерода; д) азота; е) кислорода; ж) хрома; з) марганца. [8]
Определить истинные массы атомов следующих элементов: а) хрома; б) марганца; в) вольфрама; г) ниобия. [9]
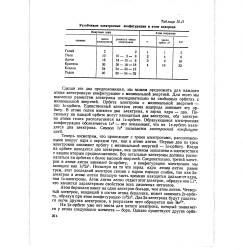 |
Устойчивые электронные конфигурации и атом водорода. [10] |
На 25-орбите уже нет места для пятого электрона, который появляется у атома следующего элемента - бора. [11]
Орбитальная модель атома водорода ( см. рис. 11) пригодна и для описания атома следующего элемента - гелия, имеющего два электрона. При этом следует учитывать, что в соответствии с принципом Паули ( см. 4.7) на каждой атомной орбитали может находиться не более двух электронов. [12]
Общая закономерность, наблюдаемая во втором периоде периодической системы, заключается в том, что каждый новый электрон в атоме следующего элемента удерживается более прочно из-за увеличивающегося заряда ядра. Поскольку остальные 2s - и 2р - электроны находятся приблизительно на таком же расстоянии от ядра, как и добавляемый электрон, он практически не экранируется ими от последовательно возрастающего положительного заряда ядра. Этот возрастающий заряд оказывает на появляющийся в атоме фтора, F, пятый 2р - электрон большее влияние, чем увеличившееся межэлектронное отталкивание. Поэтому пятый р-электрон в атоме F удерживается очень прочно и первая энергия ионизации снова возрастает. [14]
Построение простейшей модели атома водорода не представляет трудностей: один электрон вращается в нем вокруг ядра, имеющего один положительный заряд. Для атома следующего элемента периодической системы - гелия - возможны уже две различные модели; можно предположить, что два его электрона вращаются по двум орбитам, расположенным либо на разных расстояниях от ядра, либо на одинаковых. Выбор между этими двумя моделями должен быть произведен уже на основании химических свойств гелия. В самом деле, если считать правильной первую модель, то внешний электрон должен быть связан в гелии не более прочно, чем в водороде. В соответствии с этим гелий по своим свойствам должен быть похож на водород. Между тем гелий химически инертен. Это указывает на то, что оба его электрона находятся в одинаковых условиях и оба весьма прочно связаны с ядром, что и заставляет остановиться на втором варианте модели. [15]
Страницы: 1 2
