Атом - данный элемент
Cтраница 2
Все атомы данного элемента имеют одинаковое число протонов в ядре. Атомный номер Z, который определяется зарядом ядра ( выраженным в элементарных зарядах), показывает в то же время число протонов, содержащихся в ядре, и, следовательно, число электронов, вращающихся вокруг ядра. Но не все атомы одного элемента имеют одинаковое число нейтронов. Это значит, что существует несколько изотопов одного элемента. [16]
Все атомы данного элемента имеют одинаковый заряд ядра, т.е. одинаковое число протонов в ядре. Число нейтронов в ядрах атомов элемента может быть различным. Атомы, имеющие в ядрах одинаковое число протонов и различное число нейтронов, называются изото - пами. Например, природный кислород состоит из трех изотопов - ЧО [ 99 76 % ( ат. [17]
Склонность атома данного элемента к образованию двойной связи с углеродом тем меньше, чем больше объем этого атома; перекрывание р-орбит для образования тг-связи с углеродом тем менее полное, чем большим объемом обладает атом-заместитель. [18]
Способность атомов данного элемента оттягивать на себя электроны от атомов партнера более полно может быть охарактеризована, если учесть два важных показателя: энергию ионизации / и энергию электронного сродства F. [19]
Валентностью атомов данного элемента называется свойство их принимать или отда-вать строго определенное число электронов. Это свойство зависит прежде всего от числа валентных электронов: чем меньше валентных электронов, тем легче атом отдает их. Атомы инертных газов, обладающие 8 валентными электронами, не могут отдавать на одного из них. [20]
Изотопы - атомы данного элемента, ядра которых при одинаковом заряде Z имеют различные массовые числа А. [21]
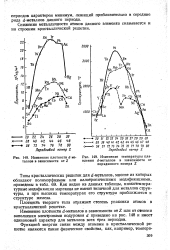 |
Изменение плотности d - ме-таллов в зависимости от Z.| Изменение температуры плавления d - металлов в зависимости от порядкового номера Z. [22] |
Снижение металличности атомов данного элемента сказывается и на строении кристаллической решетки. [23]
Эта способность атома данного элемента к оттягиванию на себя электронной плотности зависит от многих факторов ( напр. Наиболее электроотрицательны фтор, кислород, хлор. [24]
Всего у атома данного элемента 23 электрона. [25]
Зная заряд атома данного элемента, легко построить его электронную оболочку. [26]
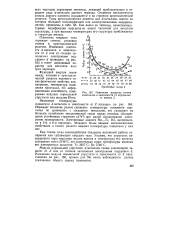 |
Изменение радиусов атомов d - металлов в зависимости от порядкового номера Z. [27] |
Снижение металличности атомов данного элемента сказывается и на строении кристаллической решетки. Как видно из таблицы, низкотемпературные модификации марганца не имеют типичной для металлов структуры, а при высоких температурах его структура приближается к структуре железа. [28]
 |
Атомы гелия ( а и кислорода ( б. [29] |
Ими определяется способность атомов данного элемента вступать в химические связи друг с другом и с атомами других элементов, а также электропроводность различных материалов. [30]
Страницы: 1 2 3 4