А-метиленовый атом
Cтраница 1
Реакционность а-метиленовых атомов водорода сильно зависит от копланарности в переходном состоянии фенильного кольца и а-атома углерода. Если в фенильное кольцо ввести несколько алкильных групп, то в тех случаях, когда эти группы не создают стерических затруднений, реакционность углеводорода складывается из реакционности отдельных групп. Например, реакционность м - и тг-цимола равна сумме реакцион-ностей толуола и изопропилбензола. Однако реакционность о-цимола значительно меньше этой суммы, так как метильная группа в о-псложении мешает изопропильной группе в переходном состоянии принять ту степень копланарности, которая осуществляется в изопропилбензоле. [1]
Полиизопрен содержит подвижные а-метиленовые атомы водорода, поэтому в принципе можно получить привитые сополимеры путем осуществления реакции передачи цепи, если инициировать полимеризацию винилового мономера в присутствии каучука. [2]
Мономеры с а-метиленовыми атомами водорода с трудом полимерп-зуются но радикальному механизму. Алилацетат, 1-октен, пропилен, иао-бутилен и изопропилацетат полимеризуются с трудом, причем образуются соединения с низким молекулярным весом. [3]
Радикалы MS и Ка-Sx, по-видимому, имеют близкую реакционную способность в реакциях отрыва а-метиленового атома водорода и присоединения по двойной связи. [4]
Было найдено, что в получающемся циклогексене-й 2 90 % атомов дейтерия локализовано на а-метиленовых атомах углерода. [5]
Для систем с изолированными двойными связями, к которым относятся и полидиены, преобладающим является отрыв а-метиленового атома водорода. [6]
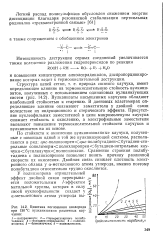 |
Кинетика поглощения кислорода при 130 С вулканизатами различных каучуков. [7] |
Сравнение строения полибутадиена с полиизопреном позволяет понять причину различной скорости их окисления. Двойная связь снижает плотность электронного облака у а-метиленового атома углерода, именно поэтому полибутадиен относительно трудно окисляется. [8]
Взаимодействие нитрозоперфторсоединений с фторзамещен-ными алкенами может привести к оксазетидинам, например ( 14) ( уравнение 42), через ион-радикальные промежуточные соединения [67] и к сополимерам, образующимся преимущественно при низких температурах. В случае алкенов, не имеющих фторированных заместителей, но содержащих а-метиленовые атомы водорода, возможен дальнейший гидролиз до ненасыщенных гид-роксиламинов. Из нефторированных соединений оксазетидины обычно не образуются [68], хотя из нитрозобензола и тетрамето-ксиэтилена был получен 3 3 4 4-тетраметокси - 2-фенил - 1 2-оксазети-дин. Арилалкены дают нитроны [68], например ( 15) [ уравнение 43 ], формально за счет расщепления двойной связи в алкене; в случае реакции со стиролом был обнаружен неустойчивый промежуточный продукт ( 16), который распадается с образованием бензилиден - Л / - фенилнитрона. Аддукты ( 17) и ( 18) идентифицированы как продукты взаимодействия нитрозотрифторметана со стиролом и трифторстиролом, соответственно. [9]
Дрисдейл и Марвел [150] исследовали процессы поперечного сшивания при эмульсионной полимеризации бутадиена и обнаружили, что при инициировании 2 2 -азобисизобутиронитрилом коэффициент полимеризации в точке гелеобразования выше, чем при инициировании персульфатом калия. При полимеризации в эмульсии реакция передачи цепи через полимер ( отрыв водорода от а-метиленового атома углерода) протекает с незначительной скоростью и, следовательно, не может привести к образованию сшитых полимеров. Образование поперечных связей происходит в основном в результате взаимодействия полимерных радикалов с остаточными двойными связями полимерных молекул. [10]
Вулканизация является результатом взаимодействия полимеров с вулканизующими агентами. Реакционная способность этих полимеров к действию вулканизующих агентов связана с наличием в них этиленовой ненасыщенности и ее активирующим влиянием на аллильные или а-метиленовые атомы водорода. Такой индуктивный эффект наблюдается и в простейших молекулах. Например, к пропилену бром присоединяется в два раза быстрее, чем к этилену. Благодаря индуктивному влиянию метальной группы натуральный каучук вулканизуется быстрее и требует меньших дозировок ускорителя и более низкой температуры вулканизации, чем бутадиен-стирольный и бутадиеновый каучуки, не содержащие боковых метальных групп. [11]
В качестве доказательства использовались данные об ингиби-рующем действии тиофенола на радикальную реакцию и об отсутствии его влияния в случае термической реакции. Однако при этом упускалось из виду, что фентиильный радикал ( C6H5S -), являясь достаточно инертным при 130 С, мог служить передатчиком цепи, отрывая а-метиленовые атомы водорода при 180 - 240 С. [12]
При использовании ускорителей основного характера следует признать в первую очередь наличие ионных реакций в полимерной цепи. Таким образом, при воздействии амина на полимерную цепь после деформации электронного облака у двойной связи может произойти поляризация; при этом соответствующая часть каучуковой цепи становится реакционноспособной. Следствием может быть дегидрирование а-метиленового атома углерода и замещение активированной молекулы серы. [13]
Замена алкильных заместителей на винильные и фенильные увеличивает реакционность. К сожалению, имеется мало данных, которые позволили бы непосредственно сравнить влияние этих групп. Все же, по-видимому, винильная группа оказывает более сильное влияние, чем фенильная. Реакционность а-метиленовых атомов водорода еще больше возрастает в циклических соединениях. Влияние алкильных, винильных и фенильных групп на реакционность атомов водорода находится в соответствии с их влиянием на энергию сопряжения в образующихся радикалах. Бросается, однако, в глаза одно несоответствие. Энергия отрыва атома водорода в толуоле и пропилене равна - 11 ккал молъ, а от метиленовой группы алканов - - - 95 ккал / моль. Как указывалось выше, толуол и пропилен не укладываются на прямую Поляни для алканов. [14]
Замена алкильных заместителей на винильные и фенильные увеличивает реакционность. К сожалению, имеется мало данных, которые позволили бы непосредственно сравнить влияние этих групп. Все же, по-видимому, винильная группа оказывает более сильное влияние, чем фенильная. Реакционность а-метиленовых атомов водорода еще больше возрастает в циклических соединениях. Влияние алкильных, винильных и фенильных групп на реакционность атомов водорода находится в соответствии с их влиянием на энергию сопряжения в образующихся радикалах. Бросается, однако, в глаза одно несоответствие. Энергия отрыва атома водорода в толуоле и пропилене равна - 77 ккал / моль, а от метиленовой группы алканов-95 ккал / моль. Как указывалось выше, толуол и пропилен не укладываются на прямую Поляни для алканов. [15]
Страницы: 1