Лигандный атом
Cтраница 1
Ряду лигандных атомов с включением других элементов может быть поставлен в соответствие новый ряд натуральных чисел. [1]
Благоприятное размещение лигандных атомов, обеспечивающее беспрепятственное контактирование, так что разрывы и ( или) перекрывания не превышают 0 3 - 0 4 А. [2]
 |
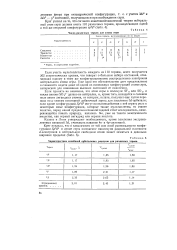
Число представителей составных r - дентатных систем. [3] |
Первые три составные системы среди г лигандных атомов содержат одновременно по меньшей мере один элемент из левой группы ( числа, стоящие слева от вер тикальной черты) и один из правой; в последней составной системе в контур обязательно входят элементы каждой из трех выделенных групп. [4]
 |
Число различных термов для атома серы.| Характеристика колебаний орбитальных радиусов для различных термов. [5] |
Если принять во внимание, что атом серы в молекуле SF6 или SO3, а также анионе SO 42 - далеко не нейтрален, и, кроме того, находится в силовом поле шести лигандных атомов, от которых, кстати, получает еще путем переноса по я-связям некоторый добавочный заряд для заселения Зс ( - орбитали; если кроме конфигурации 5рЫ2 могут во взаимодействии с ней играть роль и некоторые иные конфигурации, которые также мультиплетны, то станет понятно, перед какой предельно сложной задачей стоит исследователь, намеревающийся понять природу, казалось бы, уже не такого экзотического вещества, как серный ангидрид или серная кислота. [6]
Наконец, происходит нечто совершенно новое, недоступное свободному атому: а) на упрочненную сжатием Sd-вакансию центрального атома переходит не только путем возбуждения часть зарядовой плотности его собственных 3s - и Зр-электронов, но и с лигандных атомов ( О, F, C1) по направлению л-связей переносятся частично заряды уединенных электронных пар; б) после этого достаточно сжатые и заселенные Зс. [7]
Наблюдаемая взаимосвязь между знаком кругового дихроизма в области, соответствующей переносу заряда, и хиральностью диаминной цепи независимо от абсолютной конфигурации хелатных колец около иона металла свидетельствует о том, что имеющиеся в настоящее время теории [20-23], которые объясняют оптическую активность комплексов металлов исключительно отклонениями лигандных атомов или их орбиталей от октаэдрического расположения, имеют ограниченное применение. [8]
Сжатие, ведущее к углублению не только геометрического, но и энергетического уровня, можно условно рассматривать происходящим как бы в несколько стадий: а) возбуждение 3s - и 3 / э-электронов, б) катионизация атомов Р или S по cr - связи и перенос поя-связи, в) перекрывание с электронными облаками лигандных атомов. [9]
 |
Характеристика агрегатных состояний интергалидов. [10] |
Хлор имеет в своем третьем электронном слое пустые d - вакансии, а это ослабляет взаимное отталкивание его электронов которое еще слабее у брома и особенно мало у иода. В лигандных атомах фтора, наоборот, замечается сильное взаимное отталкивание пар электронов, составляющих внешнюю, насыщенную и не имеющую пустых вакансий оболочку. [11]
При составлении символических обозначений плоских циклов с ответвлениями начало и направление обхода ( ли-гандный или узловой атом цикла) определяют топологией ( табл. 3) и ( или), как и в случае циклов без ответвлений, по характеристике бидеьтатных элементов, составляющих цикл, основываясь на ПНЧ. При этом каждый лигандный атом получает определенный порядковый номер. Эти номера далее используются для размещения символов химического состава лигандных групп. [12]
Чрезмерное усложнение молекулы, недостаточная жесткость структуры, возникновение относительно непрочных макроциклов при хелатообразовании являются недостатками экстрагентов типа III. При надлежащем выборе лигандных атомов и подводящей их цепи возможно получение хелантов, обладающих сравнительно простым строением, почти любой требуемой степенью жесткости структуры, планарностью молекулы и способностью к образованию только 5 - и 6-членных металлоциклов. [13]
Ниже приводятся некоторые основные результаты проведенного нами анализа важнейших плоских жестких систем. Вместе с тем были рассмотрены также некоторые необычные системы ( например системы с пятью и шестью лигандными атомами, лежащими в одной плоскости), которые, возможно, будут обладать новыми особыми свойствами. [14]
Соединения, которые образуются при взаимодействии акцепторов и доноров электронов, называют комплексами, или координационными соединениями. Если взаимодействующий с акцептором реагент, который называют лигандом или лигандной группой, содержит два пли более атомов с донорными свойствами, лигандных атомов, то образующееся соединение содержит один или несколько циклов. Соединение этого типа называют хелатом, а лиганд - хелатообразующим реагентом, или хелатным лигандом. Однако не всякий лиганд, содержащий несколько донорных атомов, является хелатообразующим реагентом. Для этого необходимо такое расположение донорных атомов, чтобы они могли координироваться одним и тем же центральным атомом. Так, например, гидразин H2N - NH2 с двумя донорными атомами координируется только одним атомом азота, в то время как этилендпамин H2N - GHz - - СН2 - NH2 - одновременно обоими атомами азота. В гидразине расстояние между двумя донорными атомами слишком мало для того, чтобы была возможна координация обоих атомов азота без искажения связи между ними, в то время как в этилендиамине это расстояние достаточно велико. Таким образом, это требует вполне определенного размера хелатного цикла ( разд. [15]
Страницы: 1 2