Крепость - серная кислота
Cтраница 2
Основными переменными при очистке серной кислотой являются: относительное количество и крепость серной кислоты, температура и время контакта. [16]
Этот же кетон начинает преобладать в смеси карбонильных соединений при увеличении крепости серной кислоты ( табл. 80); в случае концентрированной серной кислоты он оказывается единственным продуктом реакции. [17]
Этот же кетон начинает преобладать в смеси карбонильны; соединений при увеличении крепости серной кислоты ( табл. 83) в случае концентрированной серной кислоты он оказывается един ственным продуктом реакций. [18]
Именно с этой точки зрения рассматривает А. И. Титов причины понижения скорости нитрования многих соединений серно-азотной кислотной смесью при велнчснин крепости серной кислоты выше некоторого значения. Величина скорости реакции нитрования определяется природой нитруемого соединения, способного реагировать не только с азотной, но и с серной кислотой. Реакция с серной кислотой в присутствии азотноп кислоты протекает только при избытке первой. [19]
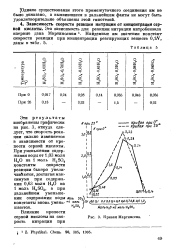 |
Кривая Мартинсена. [20] |
Эти результаты изображены графически на рис. 3, откуда следует, что скорость реакции сильно изменяется в зависимости от крепости серной кислоты. [21]
Именно с этой точки зрения Титов и Ингольд рассматривают причины понижения константы скорости нитрования многих соединений серно-азотной кислотной смесью при увеличении крепости серной кислоты выше некоторого значения. [22]
Скорость поглощения этиленовых углеводородов серной кислотой с образованием алкилсерных кислот зависит от различных факторов, важнейшими из которых являются природа углеводорода и крепость серной кислоты. Так, например, 90 % - ная серная кислота практически вовсе не поглощает этилена, тогда как изобутилен легко поглощается уже 54 % - ной кислотой. На этой разнице в отношении к серной кислоте различных этиленовых углеводородов основано промышленное получение спиртов из газов крекинга без предварительной их ректификации. Смесь газов пропускают сначала в скруббер, орошаемый 55 - 58 % - ной сорной кислотой. Аналогичным образом для поглощения пропилена применяют 85 % - ную серную кислоту, для этилена же - 98 % - ную. [23]
Скорость поглощения этиленовых углеводородов серной кислотой с образованием алкилсерных кислот зависит от различных факторов, важнейшими из которых являются природа углеводорода и крепость серной кислоты. Так, например, 90 % - ная серная кислота практически вовсе не поглощает этилена, тогда как изобутмлен легко поглощается уже 54 % - ной кислотой. На этой разнице в отношении к серной кислоте различных этиленовых углеводороде основано промышленное получение спиртов из газов крекинга без предварительной их ректификации. Смесь газов пропускают сначала в скруббер, орошаемый 55 - 58 % - ной серной кислотой. Аналогичным образом для поглощения пропилена применяют 85 % - ную серную кислоту, для этилена же - 98 % - ную. [24]
Фильтр задерживает туманообразную серную кислоту в случае попадания ее из отделения очистки или возникновения в сушильной башне при нарушении режима ее работы ( изменение крепости серной кислоты и повышение температуры) и брызги серной кислоты при плохой работе брызго-уловителя после сушильной башни. [25]
В 1788 г. Кавендиш выступил с интересной работой, которая особенно характеризует его роль в развитии методов количественного химического анализа. Эта работа посвящена определению крепости серной кислоты. [26]
Из свойств серной кислоты мы знаем, что температура паров кипящей серной кислотой и содержание в них H2SO тем выше больше крепость серной кислоты. Самая крепкая кислота в: р, 1Рате находится в котле. Пары этой кислоты при входе в де-дерриатор на первой нижней полке встречают относительно более, йшабую кислоту и, следовательно, кипящую при более низкой тем яперт ре; рри этом пары будут конденсироваться, и за счет теплота квнвврсадии их будет нагреваться кислота на нижней полке. [27]
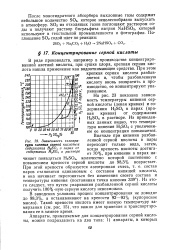 |
Зависимость температуры кипения серной кислоты и содержания H SO в парах от содержания Я25О4 в растворе. [28] |
На рис. 23 показана зависимость температуры кипения серной кислоты ( левая кривая) и содержания H2SO4 в парах ( правая кривая) от содержания H2SO4 в растворе. Из приведенных данных видно, что температура кипения H2SO4 с увеличением ее концентрации повышается. Вначале при кипении разбавленной серной кислоты в пары переходит только вода, затем, когда крепость кислоты достигает 70 %, при кипении в парах начинает появляться H2SO4, количество которой постепенно с повышением крепости серной кислоты до 98 3 % возрастает. Из этого следует, что путем упаривания разбавленной серной кислоты получить 100 % - ную серную кислоту невозможно. [29]
Графически отработка кислоты в течение цикла по мере поступления сырья, представляется более или менее плавной кривой ( рис. 9 и 10) независимо от природы перерабатываемого сырья: в одном случае сырьем является смесь бутан-бутиленовых фракций каталитического и термического крекинга, в другом, кроме названных, отработанная бутан-бутиленовая фракция и изобутан. Начальные и конечные концентрации кислоты примерно одинаковы. Резкое падение крепости серной кислоты при изменении соотношения компонентов в сырье от 1: 15 до 1: 7 с 25 / VII на 26 / VII ( рис. 9) является лишним доказательством того, что при снижении этого соотношения сокращается срок жизни кислоты. [30]
Страницы: 1 2 3