Кривая - заряжение
Cтраница 2
На кривой заряжения рения водородная область сливается с кислородной, поэтому выделить на ней водородный участок затруднительно. [16]
 |
Изотермы адсорбции водорода на Pt / Pt-электроде при различных температурах. [17] |
По кривым заряжения рассчитывают изотермы адсорбции водорода методом, который был описан в работе 1, предполагая, что независимо от температуры полное заполнение поверхности адсорбированным водородом достигается при его парциальном давлении, равном 1 атм. При повышенных температурах необходимо учитывать, что вследствие увеличения давления паров воды парциальное давление водорода понижается, а потому следует вводить поправку ( см. § 1.1) на давление паров воды, воспользовавшись табличными данными. Так как с повышением температуры растворимость водорода падает, можно уменьшать значение Ег, начиная с которого снимают кривые заряжения. [18]
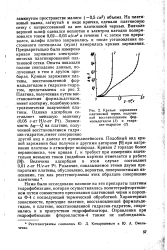 |
Кривые заряжения платиновой черни, полученной восстановлением формальдегидом ( / и гидразин-гидратом ( 2. [19] |
Подобный вид кривой заряжения был получен и другими авторами [9] при нагревании платины в атмосфере водорода. [20]
Кислородный участок кривой заряжения примерно вдвое длиннее водородного. С учетом того, что при адсорбции одного атома кислорода освобождаются два электрона, это означает, что в конце области адсорбции кислорода ( - 1 5 - 1 6 В) на один атом платины приходится примерно один атом кислорода. Следует отметить, что в кислородной и водородной областях часть электричества расходуется также на заряжение двойного слоя. [21]
Кислородная область кривой заряжения на платине имеет длину примерно в два раза больше, чем длина водородной области. [22]
Кислородная область кривой заряжения на платине имеет длину примерно в два раза больше, чем длина водородной области. Так как для адсорбции одного атома кислорода требуется два электрона, а на ионизацию атома водорода - один электрон, то отсюда можно сделать вывод, что в конце кислородной области при qv я 1 5 - г - 1 6 в число адсорбированных атомов кислорода оказывается таким же, как число атомов водорода в начале кривой заряжения. [23]
Кислородная область кривой заряжения на платине имеет длину примерно в два раза больше, чем длина водородной области. [24]
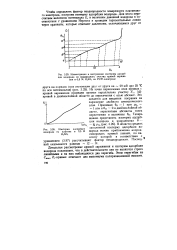 |
Иллюстрация к построению изотермы адсорбции водорода из водородного участка кривой заряжения в 0 5 М H2SO4 на Pt / Pt-электроде.| Изотерма адсорбции. [25] |
Детальное рассмотрение кривой заряжения и изотермы адсорбции водорода показывает, что в действительности они не являются строго линейными и на них наблюдаются два перегиба. [26]
Кислородная область кривой заряжения на платине имеет длину примерно в два раза больше, чем длина водородной области. [27]
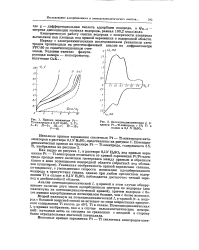 |
Кривые заряжения Pt. [28] |
Указанная необратимость кривой заряжения связана, по-видимому, с уменьшением скорости ионизации адсорбированного водорода в присутствии титана, однако при любом процентном содержании Ti в сплаве в 0 12V H2SO4 наблюдается достаточно четкий переход к двойнослойной области. [29]
При получении кривой заряжения определяют внешний заряд Q n - Для расчета реального количества адсорбированного водорода Ан необходимо учитывать заряд QS. M, определенный, например, с помощью адсорбционных измерений. Кривая 3 представляет собой зависимость Лн от потенциала. Так как по уравнению (12.54) определяется только Д / 4Н, а не абсолютное значение Ан, то при построении этой кривой сделано предположение, что в конце водородного участка кривой заряжения ( точки р, на кривой / или Рз на кривой 3) адсорбция водорода Ан равна нулю. [30]
Страницы: 1 2 3 4 5