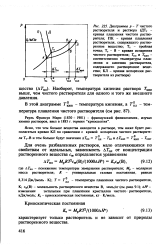
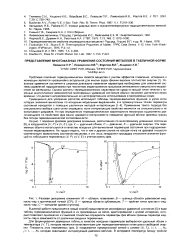
Кривая - испарение
Cтраница 4
Ясно, что чем больше вещества находится в растворе, тем ниже будет располагаться кривая КЛ по сравнению с кривой испарения чистого растворителя ТТ-В и тем больше будут значения ДТ Тпя - Гщ, и ДГКИП Г, - Гкип. [47]
Количество этана можно определить следующим графическим способом: по линии давлений графика проводим горизонтально 1 7 кГ / см. от кривой испарения пропана до кривой испарения этана и воспользуемся линейностью графика температур ( график давлений логарифмический) как масштабной линейкой. Запишем температуру, при которой эта линия пересекается кривой испарения этана - 79 С и кривой испарения пропана - 25е С. Промежуток между ними равен 79 - 25 54 С, а промежуток от - 30 С равен 30 - 25 5 С. [48]
 |
Диаграмма со. [49] |
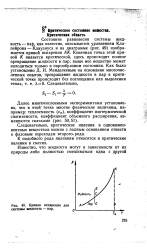
Кривые отвечают равновесию между соответствующими двумя фааами / КрЯТШГ ОС характеризует зависимость давления насыщенного пара жидкой воды от температуры и называется кривой испарения; кривая 0В - зависимость температуры замерзания воды от внешнего давления и называется кривой плавления; кривая О А - зависимость давления насыщенного пара лКда от температурьГТГ назьТ - вается кривой ВОЭРШЩИ. [50]
Кривая равновесия жидкость - пар ( кривая испарения) может быть определена прибором, изображенным на рисунке 6.2. Очевидно, на кривой испарения крайняя точка со стороны низких температур соответствует температуре отвердевания жидкости под давлением ее насыщающего пара; эту точку называют тройной точкой. [51]
 |
Кривая давления пара жидкости. [52] |
Легко убедиться, что при одной и той же температуре кривая возгонки должна иметь больший угловой коэффициент ( подниматься круче), чем кривая испарения. Определим значение dp / dT из уравнения Клаузиуса-Клапейрона, взятого в первой форме (III.1), для обоих процессов. [53]
 |
Кривая испарения для системы жидкость - пар. Q. [54] |
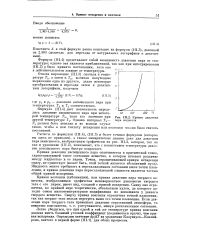
Состояние равновесия системы жидкость - пар, как известно, описывается уравнением Клапейрона - Клаузиуса и на диаграмме ( рис. 49) изображается кривой испарения АК. Конечная точка этой кривой / С является критической, здесь происходит полное превращение жидкости в пар; выше нее вещество может находиться только в парообразном состоянии. [55]
На диаграмме состояния ( Р Т) ( рис. 15.14) найденные результаты выражаются в смещении вправо и вниз кривой испарения раствора относительно кривой испарения чистого растворителя. [56]
В данной работе предлагается новый способ представления многофазных уравнений состояния [5] в виде таблиц термодинамических функций и их производных на сетке, адаптированной к кривой испарения, который позволяет однозначно и с высокой точностью определять параметры фаз вблизи границы перехода жидкость-пар в зависимости от различных входных переменных. [58]
Количество этана можно определить следующим графическим способом: по линии давлений графика проводим горизонтально 1 7 кГ / см. от кривой испарения пропана до кривой испарения этана и воспользуемся линейностью графика температур ( график давлений логарифмический) как масштабной линейкой. Запишем температуру, при которой эта линия пересекается кривой испарения этана - 79 С и кривой испарения пропана - 25е С. Промежуток между ними равен 79 - 25 54 С, а промежуток от - 30 С равен 30 - 25 5 С. [59]
Исследование процессов испарения при различных постоянных концентрациях показало, что с уменьшением концентрации ей теплоемкость в процессе кипения убывает более равномерно, в результате чего кривая испарения в i - - координатах имеет меньшую кривизну. [60]
Страницы: 1 2 3 4