Кривая - насыщение
Cтраница 1
Кривая насыщения построена по новейшим экспериментальным данным обычными методами, так же как и таблицы термодинамических свойств воды. [1]
Кривая насыщения является важной характеристикой вещества, необходимой для расчета многих его термодинамических свойств. Для этой цели было бы наиболее удобно иметь ее аналитическое выражение. Такое выражение может быть получено на основании уравнения Клапейрона - Клаузиуса, однако для этого надо знать зависимость теплоты парообразования V - и. Обычно эти зависимости не известны, и для выяснения характера кривой насыщения прибегают к тем или иным упрощениям. [2]
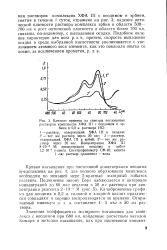 |
Влияние времени на спектры поглощения растворов комплексов ХФА III с неодимом и эрбием в 0 2 н. растворе НС1. [3] |
Кривая насыщения при постоянной концентрации неодима представлена на рис. 4; для полного образования комплекса необходим по меньшей мере 2-кратный молярный избыток реагента. [4]
Кривая насыщения показана слева пунктиром с точкой. Верхняя ее часть от критической точки относится к сухому насыщенному пару, а нижняя - к жидкости. [5]
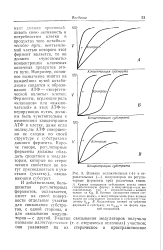 |
Влияние положительных ( и отрицательных ( - модуляторов на регуляторные ферменты трех различных типов. [6] |
Кривая насыщения субстратом всегда имеет гиперболическую форму, и модуляторы - как положительные, так и отрицательные - влияют только на К. Кривые насыщения имеют сиг-моидпую форму, и модуляторы здесь тоже влияют только на кажущееся сродство к субстрату - величину S0i5, В. [7]
Кривая насыщения р1 делит диаграмму на две части: выше ее водяные пары, содержащиеся в воздухе, не насыщены ( в перегретом состоянии), а ниже ее - в состоянии пересыщения. Так как состояние пересыщения является неустойчивым и обычно сопровождается конденсацией, то ниже предельной кривой находится бласть тумана. [8]
Кривая насыщения показана слева пунктиром с точкой. Верхняя ее часть от критической точки относится к сухому насыщенному пару, а нижняя - к жидкости. [9]
Кривая насыщения является важной характеристикой вещества, необходимой для расчета целого ряда его термодинамических свойств. Для этой цели было бы наиболее удобно иметь ее аналитическое выражение. Такое выражение может быть получено на основании уравнения Клалейрона - Клаузиуса, однако для этого надо знать зависимость теплоты парообразования г и величины v - v от темшературы. [10]
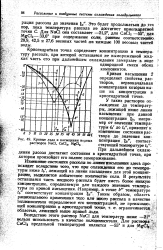 |
Кривые льда и насыщения водных растворов NaCl, СаС12. [11] |
Кривая насыщения 2 определяет свойства, растворов, первоначальная концентрация ко-дарых выше их концентрации в криогидратной точке. [12]
Кривая насыщения ф100 % делит диаграмму на две зоны: выше этой кривой расположена зона перегретого водяного пара, а ниже - зона пересыщения или тумана. Под шкалой влагосо-держаний расположена шкала парциальных давлений водяного пара. По двум параметрам воздуха можно найти на / - d - диа-грамме все остальные его параметры. [13]
Кривая насыщения является важной характеристикой вещества, необходимой для расчета целого ряда его термодинамических свойств. Для этой цели было бы наиболее удобно иметь ее аналитическое выражение. [14]
Кривая насыщения гемоглобина кислородом имеет сиг-моидную форму, поэтому гемоглобин хорошо приспособлен для связывания кислорода в легких и его освобождения в периферических тканях. Миоглобин в отличие от гемоглобина обладает значительно более высоким сродством к кислороду и характеризуется гиперболической кривой насыщения кислородом, благодаря чему он наделен способностью запасать кислород в мышцах. Эти соотношения, равно как и регулирующее воздействие связывающегося с гемоглобином 2 3-дифосфоглицерата ( ДФГ) на сродство гемоглобина к кислороду, обусловлены наличием у гемоглобина четырех специфических центров связывания с О2, СО2, ионами Н и ДФГ, а также изменениями в четвертичной структуре гемоглобина в цикле оксигенация-де-зоксигенация. Таким образом, субъединицы гемоглобина, подобно субъединицам других олигомерных белков, способны передавать сигналы о регуля-торных взаимодействиях посредством конформационных изменений молекулы белка. Изменения в аминокислотной последовательности глобулярных белков, обусловленные генными мутациями, например замена двух аминокислотных остатков в молекуле гемоглобина при серповидноклеточной анемии, могут вызвать значительные изменения конфор-мации белка и, следовательно, сказаться на его биологических функциях. [15]
Страницы: 1 2 3 4