Кривая - общее давление
Cтраница 2
Положительные отклонения от закона Рауля могут оказаться настолько значительными, что на кривой общего давления насыщенного пара появляется максимум. Если энергия взаимодействия А-В больше взаимодействия А-А и В-В, то переход компонентов в газовую фазу затрудняется, и наблюдаются отрицательные отклонения от закона Рауля. Например, при смешении ацетона с хлороформом между реагентами возникает слабая водородная связь и процесс сопровождается выделением теплоты и уменьшением объема. Парциальные давления компонентов становятся меньше рА - М р, рвЛ / В) Ов зависимость парциальных и общего давлений дара над жидкой смесью выражается вогнутыми кривыми. [16]
При больших различиях в свойствах компонентов наблюдаются положительные или отрицательные отклонения от линейной зависимости, а на кривой общего давления появляется максимум или минимум. [17]
Для растворов, которые значительно отклоняются от идеальных, Леви сохраняет две константы рядов Маргулеса и для определения их из конечных наклонов кривой общего давления пользуется методом Маргулеса, применяя скорее аналитический, чем графический метод. [18]
 |
Общее и парциальные давления pfn - паров над смесью взаимно нерастворимых жидкостей. [19] |
Равновесные данные для жидкостей с отрицательным отклонением от закона Рауля аналогичны представленным на рис. 6.2, но положение экстремальных точек при этом обратное: кривая общего давления П ( х) при ХА имеет минимум, а кривая температуры кипения, наоборот, максимум. Кривая равновесного состава фаз пересекает диагональ также при ХА. Следовательно, и для азеотропных смесей с отрицательным отклонением от закона Рауля состав равновесных паров равен составу жидкости. В отличие от равновесной кривой, представленной на рис. 6.2, для жидкостей с отрицательным отклонением при х ХА в паровой фазе летучего компонента меньше, чем в жидкости, а при х ХА летучего в парах становится больше, чем в жидкой смеси. [20]
Монотонность кривых парциальных давлений для этой системы нарушена. Кривая общего давления в зависимости от состава паровой фазы имеет ясно выраженный экстремум в точке А. Если способом, описанным выше, находить равновесные составы пара и жидкости, то можно заметить, что по мере приближения к точке А состав паровой и жидкой фаз сближаются и, наконец, в точке А сделаются одинаковыми. Следовательно, в точке А состав жидкой и паровой фаз становится одинаковым. Эта точка носит название точки нераздельного кипения или азеотропной точки. [21]
Очень характерно течение кривых парциальных давлений в верхней части ( линей - Фиг. Рауля; кривые общего давления проходят через минимум, и в этом экстремуме состав пара и жидкости одинаков. [22]
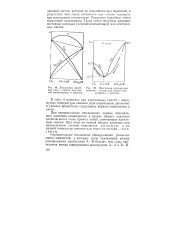 |
Диаграмма давление пара - состав для смесей сероуглерода и ацетона.| Диаграмма температура кипения - состав для смесей сероуглерода и ацетона. [23] |
При отрицательных отклонениях кривые парциального давления компонентов и кривая общего давления располагаются ниже прямых линий, отвечающих идеальным смесям. При этом на кривой общего давления при определенном составе появляется минимум, а на кривой температур кипения для этого же состава - максимум. [24]
При положительных отклонениях кривые парциальных давлений жидкостей, а также общего давления располагаются выше прямых линий, соответствующих идеальному случаю. При достаточно сильных отклонениях от закона Рауля на кривой общего давления при определенном составе появляется максимум. [25]
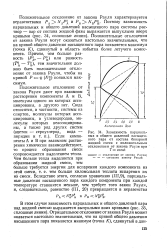 |
Зависимость парциальных и общего давлений насыщенного пара от состава бинарной жидкой смеси с положительным отклонением от закона Рауля при Т const. [26] |
Положительное отклонение от закона Рауля характеризуется неравенствами РА NAP A и Рв ] NBP B. Положительные отклонения от закона Рауля могут оказаться настолько значительными, что на кривой общего давления насыщенного пара появляется максимум ( точка К), сдвинутый в область избытка более летучего компонента. Причем, чем больше разность ( Р А - Р в) или разность ( Т А - Т ъ), тем значительнее должно быть положительное отклонение от закона Рауля, чтобы на кривой Р ф ( N) появился максимум. [27]
Очевидно, что точка перегиба на кривой общего давления пара может быть граничной точкой для области существования азеотропа. По всей вероятности можно считать, что данные работы [244] указывают на существование точки перегиба на кривой общего давления ( Р - состав) для системы вольфрам - кислород при температурах 1550 - 1600 К. [28]
 |
Диаграмма давления паров в системе метилаль - сероуглерод. [29] |
Существуют азеотропные смеси и другого рода. Кривая общего давления лежит выше идеальной пря-мой. При достаточной величине этих отклонений на кривой общего давления пара может образоваться максимум. [30]
Страницы: 1 2 3