Зарядная кривая
Cтраница 3
На рис. 27 и 28 показаны типичные зарядные кривые НК и НЖ аккумуляторов. [31]
 |
Типичные зарядные кривые ламельных никель-кадмиевых аккумуляторов при температуре 20 С. [32] |
На рис. 25 и 26 показаны типичные зарядные кривые НК и НЖ аккумуляторов. [33]
Как видно из рисунка, на зарядной кривой аккумулятора имеются две ступени. [34]
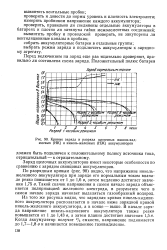 |
Кривые заряда и разряда щелочных никель-кадмиевых ( НК и никель-железных ( НЖ аккумуляторов. [35] |
Из того же рисунка видно, что зарядная кривая никель-кадмиевого аккумулятора располагается в начале ниже зарядной кривой никель-железного аккумулятора, а в конце - выше. Когда аккумулятор получит 2 / 3 емкости, напряжение поднимается до 1 7 - 1 8 в и начинается повышенное газовыделение. [36]
Внешне зарядная кривая кислотного аккумулятора очень похожа на зарядную кривую серебряно-цинкового аккумулятора, у нее также имеются две явно выраженные ступени, правда с иным соотношением их длительностей. Отличием является, кроме того, наличие в начале зарядной кривой небольшого участка с более резким повышением напряжения, а также то, что первая ступень не является строго горизонтальной, как у серебряно-цинкового аккумулятора. [37]
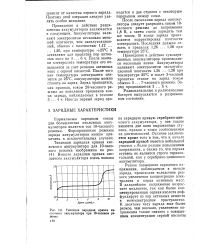 |
Типичная зарядная кривая кислотного аккумулятора при 10-часовом ре. [38] |
Отличие заключается кроме того в том, что в начале зарядной кривой имеется небольшой участок с более резким повышением напряжения, а также то, что первая ступень не является строго горизонтальной, как у серебряно-цинкового аккумулятора. [39]
Ввиду того, что процесс восстановления железа идет с заметным перенапряжением, зарядная кривая лежит при значительно более электроотрицательных значениях потенциала, чем разрядная. Это явление наряду с небольшим перенапряжением водорода на железе приводит к совместному с железом выделению водорода. Однако рост величины перенапряжения водорода на железе от плотности тока больше роста перенапряжения железа на железе, поэтому заряд железо-никелевых аккумуляторов необходимо проводить при повышенных плотностях тока, так как при малых плотностях тока возможен недозаряд активной массы отрицательного электрода. [40]
Контроль напряжения при заряде не позволяет определить с достаточной точностью окончание процесса, поскольку зарядная кривая имеет пологий характер без четких участков постоянного напряжения, которые наблюдаются при заряде свинцовых или серебряно-цинковых аккумуляторов. Это связано с тем, что побочные реакции образования кислорода и водорода протекают соответственно в области потенциалов восстановления гидроксида железа ( II) и окисления гидроксида никеля ( II) и поэтому начинают сопровождать основные электродные реакции уже на ранней стадии заряда. [41]
Во время заряда аккумулятора при повышении его напряжения до уровня, соответствующего второй ступени зарядной кривой, на поверхности серебряного электрода начинает формироваться переходный барьер, в результате чего сопротивление электрода возрастает. В момент образования переходного барьера сопротивление электрода достигает максимальной величины. При дальнейшем окислении электрода сопротивление его падает до величины, характерной для протекания второго анодного процесса, вследствие увеличения на поверхности пор концентрации высшего окисла. [42]
Из того же рисунка видно, что зарядная кривая никель-кадмиевого аккумулятора располагается в начале ниже зарядной кривой никель-железного аккумулятора, а в конце - выше. Когда аккумулятор получит 2 / 3 емкости, напряжение поднимается до 1 7 - 1 8 в и начинается повышенное газовыделение. [43]
Во время заряда аккумулятора при повышении его напряжения до уровня, соответствующего второй ступени зарядной кривой па поверхности серебряного электрода начинает формироваться переходный барьер, в результате чего сопротивление электрода возрастает. В момент образования переходного барьера сопротивление электрода достигает максимальной величины. При дальнейшем окислении электрода сопротивление его падает до величины, характерной для протекания второго анодного процесса, вследствие увеличения на поверхности пор концентрации высшего окисла. [44]
Таким образом, при уменьшении зарядного тока величина отношения максимального сопротивления к сопротивлению аккумулятора на второй ступени зарядной кривой снижается. [45]
Страницы: 1 2 3 4 5