Простейший атом
Cтраница 2
Атом водорода - простейший атом, состоящий из электрона, движущегося в кулоновском поле ядра. Потенциальная энергия электрона - е2 / г описывается гиперболической воронкой ( рис. 1.1, а), в глубине которой находится протон. Это позволяет найти строгое решение уравнения Шредингера. [16]
Рассмотрим в качестве примера простейший атом - атом водорода, который состоит из ядра и одного движущегося вблизи ядра электрона. [17]
Рассмотрим некоторые возможные термы простейших атомов. Электрон атома водорода в основном состоянии обладает ls - электроном. [18]
При разработке теории строения простейшего атома - - атома водорода, для которого порядковый номер равен единице, Бор столкнулся со следующими трудностями. Следуя Резерфорду, Бор предположил, что единственный электрон в атоме водорода вращается вокруг ядра по круговой орбите. Двигаясь по окружности с постоянной тангенциальной скоростью, электрон вместе с тем должен двигаться с ускорением, так как его скорость все время должна изменять направление. А раз так, то согласно классической электродинамике электрон должен излучать энергию и двигаться не по окружности, а по спиралевидной кривой и в конце концов упасть на ядро, а атом как таковой тем самым должен прекратить свое существование. [19]
Рассмотрим некоторые возможные термы простейших атомов. [20]
Рассмотрим теперь эту связь для простейшего атома, состоящего из одного электрона и одного протона. Кроме того, используем дипольное приближение: векторный потенциал оптического поля не меняется заметным образом на расстояниях порядка размера атома. [21]
Чтобы понять строение атомов, мы рассмотрим простейший атом - атом водорода. Нам бы хотелось описать динамику движения электрона, который движется вблизи протона. Под динамикой движения подразумевается энергия электрона, импульс, траектория и изменение этих величин во времени. Можно надеяться, что такое описание поможет нам понять, почему два атома водорода соединяются и образуют молекулу Н2, но из трех атомов водорода молекула Н3 не образуется. [22]
Орбитальный / и спиновый 2 магнитные моменты простейшего атома ( атома водорода) представлены векторами на рис. 1.1. Таким образом, атом водорода можно рассматривать как элементарный магнитик, магнитный момент которого определяется суммой орбитального и спинового магнитных моментов. [23]
Создать теорию означало рассчитать структуру хотя бы простейшего атома - ядро плюс один электрон. [24]
Ознакомить с численными данными об энергетических уровнях простейшего атома, каким является атом водорода. Эти данные объясняются в следующих двух разделах на основе волновой модели. [25]
На основе этих постулатов Бору удалось построить теорию простейшего атома - атома водорода, содержащего только один электрон. Эта теория позволила объяснить установленные на опыте швейцарским учителем физики И. [26]
В этой главе рассматриваются решения уравнения Шредингера для простейшего атома. Эти решения приводят к понятию атомной орбитали, которое является фундаментальным в современной теории валентности. [27]
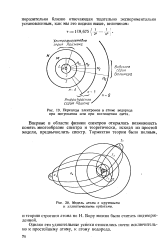 |
Переходы электронов в атоме водорода при испускании или при поглощении света.| Модель атома с круговыми и эллиптическими орбитами. [28] |
Однако эти удивительные успехи относились почти исключительно к простейшему атому, к атому водорода. [29]
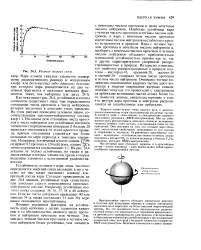 |
Ядерная энергия связи. [30] |
Страницы: 1 2 3 4